Devoirs Corrigés Physique Chimie N°3 S1 Tronc commun
Modèle N°1
Physique-Chimie • TC S biof
Durée: 2 heures
NB :
- Vous pouvez traiter les exercices dans l’ordre que vous désirez.
- Toutes les réponses devront être correctement justifiées.
- Un point est réservé à la présentation de votre copie.
PHYSIQUE (13 points)
Physique 1 : Principe d’inertie
8 points
Un mobile est en mouvement sur une table parfaitement lisse. Il est attaché à un point central A par un fil. On supposera qu’il évolue sans frottements sur cette table. Le mobile de masse \( m = 250 \, \text{g} \) est initialement en position (1). Il est attaché à un fil puis lancé. Il n’a pas le temps d’effectuer un tour complet : Le fil casse en position (5). Le mouvement du mobile est alors modifié, il se dirige vers une partie de la table rugueuse.
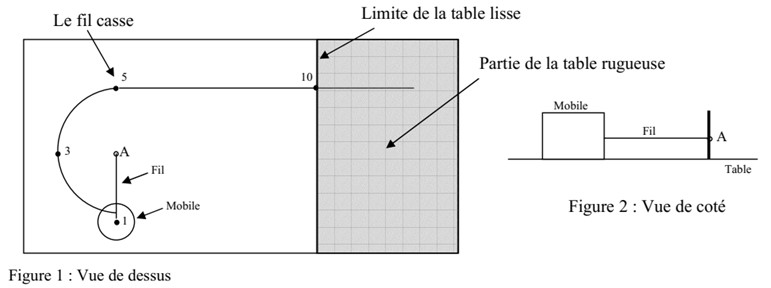
Le document ci-dessous représente l’enregistrement d’une partie du mouvement du mobile.
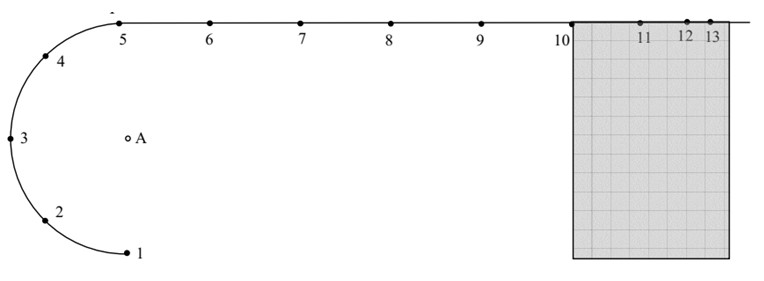
Échelle : 1 cm sur le document représente 4 cm en réalité. L’intervalle de temps entre deux positions successives vaut \( \tau = 40 \, \text{ms} \). On a numéroté les positions successives du centre G du mobile.
1 point
1,5 points
1,5 points
1 point
1 point
1,5 points
0,5 point
Physique 2 : Position de rencontre de deux mobiles
5 points
Les équations horaires des mouvements de deux mobiles A et B en mouvement sur une route droite munie d’un axe \( (x’Ox) \) sont :
\( x_A = 20t – 10 \) et \( x_B = -10t + 90 \)
avec \( x_A \) et \( x_B \) en mètre et \( t \) en seconde.
1 point
0,5 point
1 point
1,5 points
CHIMIE (7 points)
Partie 1 : Structure de l’atome
2 points
| Atome ou ion | K⁺ | O²⁻ | ||
|---|---|---|---|---|
| Nom | Ion potassium | Lithium | Ion chlorure | Ion oxyde |
| Symbole du noyau | ||||
| Charge | -e | |||
| Nombre de protons | 19 | 17 | ||
| Nombre de neutrons | 20 | 4 | 18 | 8 |
| Structure électronique | (K)²(L)¹ | (K)²(L)⁸ |
Partie 2 : Atomes et ions
Données :
Charge élémentaire : \( e = 1{,}6 \times 10^{-19} \, \text{C} \) | Masse d’un nucléon : \( m_n \approx 1{,}67 \times 10^{-27} \, \text{kg} \) | Nombre d’Avogadro : \( N_A = 6{,}02 \times 10^{23} \, \text{mol}^{-1} \)
A. L’atome de Bismuth
Le symbole de l’élément chimique Bismuth est Bi. Le noyau de son atome est constitué de 209 nucléons et sa charge est \( q = 1{,}33 \times 10^{-17} \, \text{C} \).
0,5 point
0,5 point
0,5 point
0,5 point
B. L’atome de Phosphore
Le symbole de l’élément Phosphore est P. Le noyau de son atome est constitué de 15 protons et de 16 neutrons.
1 point
0,5 point
🔒 Abonnez-vous pour accéder à la correction détaillée .
Modèle N°2
Physique-Chimie • TC S biof
Durée: 1h 50 min
NB :
- Toutes les réponses devront être correctement justifiées.
- Les calculs doivent être détaillés et les unités précisées.
- Un point est réservé à la présentation de votre copie.
CHIMIE
Partie I : Modèles de Lewis et structures électroniques
Recopier et compléter le tableau suivant : (4.5 points)
Tableau à compléter
| Atome | Structure électronique | Nombre de liaisons liantes (nt) | Nombre de liaisons libres pour chaque atome (nd) | Modèle de Lewis de la molécule CH₃Cl | Modèle de Lewis de la molécule CO₂ |
|---|---|---|---|---|---|
| \( C(Z = 6) \) | …………………… | …………………… | …………………… | …………………… | …………………… |
| \( H(Z = 1) \) | …………………… | …………………… | …………………… | ||
| \( O(Z = 8) \) | …………………… | …………………… | …………………… | ||
| \( Cl(Z = 17) \) | …………………… | …………………… | …………………… |
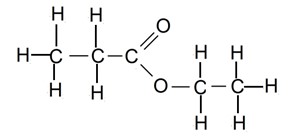
Partie II : Propanoate d’éthyle (arôme de fraise)
La formule développée ci-contre représente la molécule de propanoate d’éthyle (arôme de fraise).
PHYSIQUE
Exercice 1 : Étude d’un ressort 6,5 points
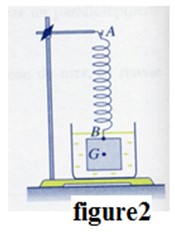
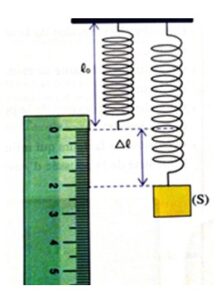
On considère un ressort de raideur \( K \) et de longueur initiale \( ℓ_0 = 7 \, \text{cm} \). On suspend à l’extrémité du ressort un solide (S) de masse \( m = 400 \, \text{g} \), et sa longueur devient \( ℓ = 11 \, \text{cm} \) (figure 1).
On donne : \( g = 10 \, \text{N/kg} \) (intensité de pesanteur).
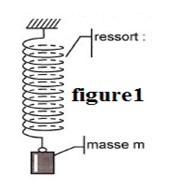
3. Maintenant, on immerge totalement le solide (S) de masse \( m = 400 \, \text{g} \) dans un liquide de masse volumique \( \rho \), on remarque que l’allongement du ressort est \( \Delta ℓ’ = 1,5 \, \text{cm} \).
Exercice 2 : Équilibre d’un solide 6 points
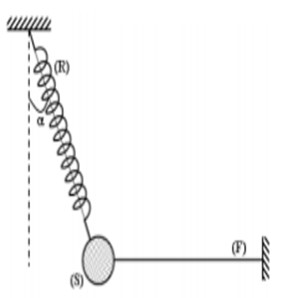
On considère un solide (S), de masse \( m = 200 \, \text{kg} \), accroché à un ressort (R) et à un fil (F) comme l’indique la figure ci-contre.
Le ressort, de constante de raideur \( k = 40 \, \text{N/m} \), est incliné d’un angle \( \alpha \) par rapport à la verticale. On donne l’allongement du ressort dans cette position \( \Delta ℓ = 10 \, \text{cm} \).
🔒 Abonnez-vous pour accéder à la correction détaillée .
Modèle N°3
Physique-Chimie • TCSF
Durée: 1h30
NB :
- Toutes les réponses devront être correctement justifiées.
- Le soin et la clarté seront pris en compte.
CHIMIE (7 points)
Cet exercice vise à tester vos connaissances sur la structure électronique des atomes et des molécules, ainsi que sur la représentation de Lewis et de Cram.
Exercice 1 : Géométrie de quelques molécules
Partie 1 :
Compléter le tableau suivant :
| Atome | Z | Structure électronique de l’atome | Règle de Duet ou de l’Octet | Structure électronique de l’ion | Symbole de l’ion |
|---|---|---|---|---|---|
| Cl | 17 | …………………………………………. | …………………………………………. | …………………………………………. | …………………………………………. |
| N | 7 | …………………………………………. | …………………………………………. | …………………………………………. | …………………………………………. |
Partie 2 :
Compléter le tableau suivant pour les molécules : PCl3, HF et CCl4.
| Molécule | Les atomes | Structure électronique | p | nt | nL | nnL | Représentation de LEWIS | Représentation de CRAM |
|---|---|---|---|---|---|---|---|---|
| PCl3 | P (Z=15) | ……… | ……… | ……… | ……… | ……… | ……… | ……… |
| Cl (Z=17) | ……… | ……… | ……… | ……… | ……… | |||
| Cl (Z=17) | ……… | ……… | ……… | ……… | ……… | |||
| Cl (Z=17) | ……… | ……… | ……… | ……… | ……… | |||
| HF | H (Z=1) | ……… | ……… | ……… | ……… | ……… | ……… | ……… |
| F (Z=9) | ……… | ……… | ……… | ……… | ……… | |||
| CCl4 | C (Z=6) | ……… | ……… | ……… | ……… | ……… | ……… | ……… |
| Cl (Z=17) | ……… | ……… | ……… | ……… | ……… | |||
| Cl (Z=17) | ……… | ……… | ……… | ……… | ……… | |||
| Cl (Z=17) | ……… | ……… | ……… | ……… | ……… | |||
| Cl (Z=17) | ……… | ……… | ……… | ……… | ……… |
Partie 3 : Molécule de 2,3-butanedione (diacétyle)
Voici le modèle moléculaire de la molécule de 2,3-butanedione (responsable du goût de beurre) :
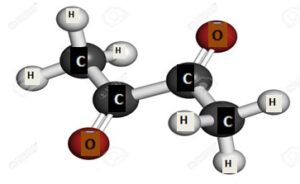
1. Quelle est sa formule brute ?
0,5 point
2. Quelle est sa formule semi-développée ?
1 point
3. Quelle est sa formule développée ?
1 point
4. Quelle est sa représentation de Lewis ?
1 point
PHYSIQUE (13 points)
Exercice 2 : Poussée d’Archimède et tension du ressort
7 points
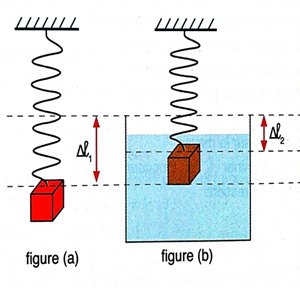
On suspend un solide cubique de masse \( m \) et d’arête \( a = 4,77 \, \text{cm} \) à l’aide d’un ressort de raideur \( K = 50 \, \text{N.m}^{-1} \). Le ressort s’allonge de \( \Delta l_1 = 10 \, \text{cm} \) (figure a).
1. En étudiant l’équilibre du solide, déterminer \( m \).
1,5 point
On trempe totalement la masse dans un liquide. L’allongement du ressort devient alors \( \Delta l_2 = 8 \, \text{cm} \) (figure b).
2. Donner le bilan des forces exercées sur le solide et représenter ces forces.
1,75 point
3. Déterminer l’intensité \( F_a \) de la poussée d’Archimède.
1,5 point
4. En déduire \( \rho \) la masse volumique du liquide.
1,5 point
5. Quel est le liquide utilisé parmi les suivants ?
0,75 point
| Liquide | Huile d’olive | Éthanol | Eau |
|---|---|---|---|
| \( \rho \, (\text{g/cm}^3) \) | 0,92 | 0,788 | 1 |
On donne \( g = 10 \, \text{N/kg} \)
Exercice 3 : Détermination de la raideur d’un ressort
6 points
On accroche un corps à l’extrémité libre d’un ressort et on mesure l’allongement \( \Delta L \) du ressort pour différentes masses \( m \). Les résultats sont consignés dans le tableau suivant :
| \( m \, (\text{kg}) \) | 0 | 0,05 | 0,1 | 0,15 | 0,20 |
|---|---|---|---|---|---|
| \( \Delta L \, (\text{m}) \) | 0 | 0,1 | 0,2 | 0,3 | 0,4 |
1. Faire l’inventaire des forces appliquées au corps. Les représenter sur un schéma.
1,5 point
2. En étudiant l’équilibre du corps, donner l’expression de la masse \( m \) en fonction de \( \Delta L \), \( K \) et \( g \).
1 point
3. Tracer la courbe \( m = f(\Delta L) \).
1,5 point
4. Déterminer la valeur de la raideur \( K \) du ressort.
2 points
On donne \( g = 10 \, \text{N/kg} \)
🔒 Abonnez-vous pour accéder à la correction détaillée .
Devoirs Corrigés Physique Chimie N°3 S1 Tronc commun
