Devoirs Corrigés Physique N°2 S1 3AC
Modèle $N°1$
Exercice 1 (8pts)
1. Remplir les lacunes par les mots qui conviennent. (4pts)
La solution aqueuse est un mélange entre un soluté et exemples des solutions aqueuses.
Le chlorure d’aluminium sa formule ; (Cu²⁺ + SO₄²⁻) son nom est
Les solutions aqueuses se classent dans trois catégories : les solutions qui ont des pH inférieures à 7 ; des solutions qui ont des pH supérieures à 7 et des solutions
2. Choisir toutes les bonnes réponses (2pts)
– Les matériaux organiques se constituent essentiellement de :
| Carbone et azote | Oxygène et carbone et azote | Hydrogène et carbone |
– Diluer une solution basique entraîne :
| Augmentation de son pH | Affaiblir de sa basicité | Diminuer sa concentration en ions OH⁻ |
– Le matériau organique est un composé tel que :
| C₃H₆O | NH₃ | H₂O |
3. Tableau des solutions (4pts)
| La solution | Jus de tomate | Ammoniaque | Eau de chaux | Eau distillée | Acide nitrique | Chlorure de sodium |
|---|---|---|---|---|---|---|
| Son pH | 4 | 12,8 | 9,3 | 7 | 1,5 | 7,00 |
| Nature de solution |
3.1. Classer dans le tableau les solutions précédentes en solution basique ; solution acide ou solution neutre
3.2. Préciser la solution la plus acide :
Préciser la solution la moins basique :
3.3. On ajoute une quantité d’acide nitrique à un volume d’eau distillée ; comment varie son pH ?
3.4. Son pH
3.5. Comment appelle-t-on cette opération ?
Exercice 2 (5pts)
Pour s’assurer des compositions des matériaux Organiques on procède à l’expérience suivante.
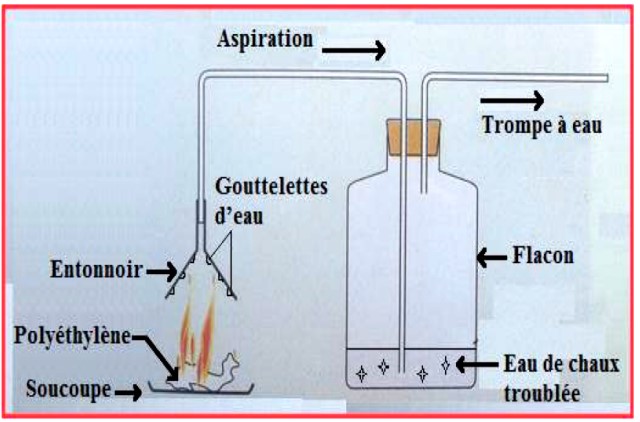
1. De quel matériau organique s’agit-il ?
Il s’agit de
2. Préciser les deux réactifs de cette combustion
1er réactif :
2ème réactif :
3. Préciser à l’aide du schéma les produits de cette combustion
1er produit :
2ème produit :
4. Quels sont les éléments nécessaires constituants un matériau organique ?
Justifier :
Exercice 3 (5pts)
Vous sortez en excursion avec vos collègues de la classe dans la forêt où vous avez trouvé une bouteille qui porte juste les deux pictogrammes suivants. Un de vos collègues a suggéré de sentir la solution pour savoir de quoi il s’agit, tandis qu’un autre a dit qu’il faut porter cette bouteille avec précaution au laboratoire du collège.
Aidez vos copains à bien se comporter avec cette solution :
1) Quel est le sens de chaque pictogramme ?
……………………………………………………………………………………….
2) Quels sont les risques encourus par cette solution ?
……………………………………………………………………………………….
3) Citer quelques précautions pour manipuler cette solution
……………………………………………………………………………………….
4) Comment peut-on se débarrasser de cette solution ?
……………………………………………………………………………………….
Modèle $N°2$
EXERCICE 1 : (8 points)
1) Répondre par vrai ou faux : (2pt)
– Le carton est une matière organique naturelle …………
– Lorsqu’on dilue une solution acide le pH diminue …………
– Une solution de pH=5 contient une abondance des ions H⁺ …………
– La solution de pH=11 est plus basique qu’une solution de pH=9 …………
2) Compléter les phrases suivantes : (2pt)
– Les ions responsables de l’acidité sont ………… tandis que celles qui sont responsables de la basicité sont …………
– Les matières organiques sont constituées essentiellement des atomes de ………… et …………
3) Situation familiale – Corrosion des métaux
Contexte : Les couteaux sont fabriqués en fer, la cocotte-minute est fabriquée en aluminium.
a) Expliquer comment la rouille s’est formée sur le couteau ? (1pt)
……………………………………………………………………..
b) Écrire l’équation de la formation de la rouille. (1pt)
……………………………………………………………………..
c) Expliquer comment la cocotte-minute a perdu son éclat métallique. (1pt)
……………………………………………………………………..
d) Citer deux techniques pour protéger le fer de l’oxydation. (1pt)
……………………………………………………………………..
EXERCICE 2 : (8 points)
On a mesuré le pH de quelques produits d’usage courant :
| Produits | Eau de Javel | Eau de chaux | Eau distillée | Jus de tomate | Détartrant |
|---|---|---|---|---|---|
| pH | 13 | 11 | 7 | 4 | 1,5 |
| Type | … | … | … | … | … |
1) Indiquer deux méthodes permettant de mesurer le pH de ces solutions ? (1pt)
……………………………………………………………………..
2) Indiquer pour chaque produit s’il est acide, neutre ou basique. Justifier (2,5pt)
……………………………………………………………………..
3) Quelle est la solution la plus acide ? Justifier (1pt)
……………………………………………………………………..
4) Quelle est la plus basique ? Justifier (1pt)
……………………………………………………………………..
5) Classer ces produits d’entretien du plus acide au plus basique. (1pt)
……………………………………………………………………..
6) Que se passe-t-il si on dilue une solution d’eau de javel avec de l’eau ? Que peut-on dire alors de son pH ? (1,5pt)
……………………………………………………………………..
EXERCICE N°3 : (4 points)
Pendant les vacances d’été, vous êtes allé avec votre famille dans une forêt. L’attention de votre frère a été attirée par un lieu où se brûlent des roues en caoutchouc, au milieu des arbres et près d’un rassemblement résidentiel. Plusieurs questions se sont alors posées à l’esprit :
Quelle est la nature du caoutchouc ? Quels sont les dangers que ce processus de combustion peut causer ?
- La formule chimique du caoutchouc est: C5H8
- Les atomes de soufre entrent dans la fabrication du caoutchouc

1) Répondez aux questions de votre frère en utilisant les documents qui se trouvent à ses côtés. (1,5pt)
……………………………………………………………………..
2) Proposez une expérience pour montrer à votre frère que le caoutchouc est organique. (1,5pt)
……………………………………………………………………..
3) Déterminez le risque de combustion incomplète des roues en caoutchouc. (1pt)
……………………………………………………………………..
Modèle $N°3$
Exercice 1 : (8pts)
1) Donner la définition de : (1 Pt)
– Le pH d’une solution : ……………………………………………………………
– Une matière organique : ……………………………………………………………
2) Répondez par « Vrai » ou « faux » (2 Pt)
| ✅ La matière organique est essentiellement constituée d’atomes de carbone C et d’atomes d’hydrogène H. | … |
| ✅ CO est un Gaz incolore toxique produit par la combustion incomplète | … |
| ✅ Lorsqu’on dilue une solution acide, son pH augmente. | … |
| ✅ Les solutions acides contiennent plus des ions H+ que les ions OH– | … |
3) Compléter les phrases par les mots qui convient : (1.5 Pt)
– La combustion …………………… produit toujours du dioxyde de carbone et de l’eau.
– On classe les solutions en trois types selon le pH : Les solutions acides de ……, les solutions basiques de …… et les solutions neutres de ……
– Les ions responsables de l’acidité sont …… tandis que celles qui sont responsables de la basicité sont ……
4) choisir les matériaux organiques parmi les suivants ? (1.5 Pt)
CH3COOH – PS – KMnO4 – PVC – C4H10 – NH3 – CH2 – C3H7OH – Fe3O4
……………………………………………………………………………………….
5) Entourer la bonne réponse ? (1 Pt)
– La formule ionique de l’acide chlorhydrique est :
(H+ + Cl–) HCl NaOH
– La Combustion de PVC, produit un gaz de formule chimique :
SO2 NO HCl
– Le pH d’une solution ionique de formule (Fe2+ + 2OH–) peut égale à :
11 4 7
– On mesure Le pH des solutions aqueuse par papier de :
pH pOH
6) Relier par des flèches ? (1 Pt)
– Produit dangereux pour l’environnement . ……………………
– Gaz toxique et mortel produit par la combustion de polyster . ……………………
– Parmi les gaz qui provoquent la phénomène l’effet de serre . ……………………
– Produit toxique, risque d’empoisonnement peut entrainer la mort ……………………
Exercice 2 : (8 pts)
PARTIE A (2.5pts)
La combustion de nylon dans le dioxygène de l’air produit : la vapeur d’eau, le dioxyde de carbone, le carbone et le cyanure d’hydrogène.
1) Citer les noms des réactifs et les produits de cette réaction ? (0.5pt)
……………………………………………………………………………………….
2) Ecrire le bilan de cette réaction ? (0.5pt)
……………………………………………………………………………………….
3) Quels sont les atomes entrant dans la composition de nylon ? (0.5pt)
……………………………………………………………………………………….
4) Le nylon est une matière organique ? justifier votre réponse ? (0.5pt)
……………………………………………………………………………………….
5) Préciser les dangers de combustion de ces types de matériaux organiques ? (0.5pt)
……………………………………………………………………………………….
PARTIE B (5.5pts)
On a mesuré le pH de quelques solutions courantes, elle a rassemblé ses résultats dans un tableau :
| La solution | Jus de tomate | Ammoniaque | Eau de chaux | Eau salée | Acide nitrique |
|---|---|---|---|---|---|
| pH | 4 | 12,8 | 9,3 | 7 | 1,5 |
| Nature de solution | … | … | … | … | … |
1) Donner deux méthodes permettant de mesurer le pH des solutions ? (0.5pt)
……………………………………………………………………………………….
2) Avec quel moyen on a mesuré le pH de ces solutions ? Justifier votre réponse ? (0.5pt)
……………………………………………………………………………………….
3) Classer dans le tableau les solutions en solution acide, basique ou neutre ? (1.25pt)
(Réponse à reporter dans le tableau ci-dessus)
4) Quelle est la solution la plus acide ? Justifier ? (0.5pt)
……………………………………………………………………………………….
5) Quelle est la plus basique ? Justifier ? (0.5pt)
……………………………………………………………………………………….
6) Classer ces solutions du plus acide au plus basique ? (1.25pt)
……………………………………………………………………………………….
7) On ajoute à 100 ml d’eau pure un volume de la solution Ammoniaque.
a- que se passe-t-il pour la valeur du pH de la solution d’Ammoniaque ? (0.5pt)
……………………………………………………………………………………….
b- Donnez le nom du processus utilisé et montrer sa rôle ? (0.5pt)
……………………………………………………………………………………….
8) Donner deux précautions lors de l’utilisation d’une solution concentrée ? (0.5pt)
……………………………………………………………………………………….
Exercice 3 : (4 pts)
Monsieur Taha a remarqué :
- Qu’il y a la formation de rouille sur son parabole de fer.
- La fenêtre d’aluminium est recouverte par une couche blanche.

1) Écrire l’équation bilan de la formation de la rouille sur le couteau (l’oxydation de fer).
……………………………………………………………………………………….
2) Expliquer pourquoi dans les villes côtières le fer est plus vite attaqué par la rouille en comparaison avec les villes qui sont loin de la mer.
……………………………………………………………………………………….
3) Expliquer pourquoi l’aluminium est utilisé sans peinture.
……………………………………………………………………………………….
4) Citer deux techniques pour protéger le fer contre la corrosion.
……………………………………………………………………………………….
Modèle $N°4$
Exercice1 : (7,5pts)
1. Compléter les phrases par les mots suivants :(2Pts)
papier pH – pH-mètre – diminue – carbone – hydrogène – dilution
a. Les matières organiques sont constituées essentiellement des atomes de ……… et ………
b. Il existe deux méthodes permettant de mesurer le pH d’une solution : le ……… et le ……… qui donne des valeurs précises.
2. Répondre par « Vrai » ou « faux » : (2Pts)
a. Le pH d’une solution basique est égal à 7.
b. L’ion responsable sur l’basicite des solutions est H+.
c. Une matière organique est constituée essentiellement du carbone et oxygène.
d. Le sel n’accélère pas l’oxydation du fer.
3. Choisir la bonne réponse : (1,5Pts)
a- On dilue une solution basique, la valeur de pH :
- □ Augmente
- □ diminue
- □ ne change pas
b- Parmi les produits de la combustion de polystyrène (PS) dans le dioxygène de l’air :
- □ HCl₂
- □ S₂O₂
- □ SO₂
c- L’eau de chaux permet de détecter :
- □ le dioxyde de carbone
- □ le monoxyde de carbone
- □ Le dioxygène
4. Relier chaque élément par sa formule ou son symbole. (2Pts)
| Alumine (……….) | Rouille (……….) | Fer (……….) | Aluminium (……….) | |
|---|---|---|---|---|
| AlO₃ | Al | Fe₂O₃ | Al₂O₃ | Fe |
Exercice 2: (9Pts)
Partie A : Les pH de plusieurs solutions
| Solution | A | B | C | D | E | F |
|---|---|---|---|---|---|---|
| pH | 13,1 | 2,6 | 11,4 | 10 | 1,2 | 7 |
| Type | … | … | … | … | … | … |
1- Compléter le tableau en déterminant le type de chaque solution (1Pt)
(Réponse à reporter dans le tableau ci-dessus)
2- Quelle est la méthode utilisée pour mesurer le pH de ces solutions ? justifier (1Pt)
……………………………………………………………………………………….
3- Déterminer la solution la moins acide et la solution la plus basique (1Pt)
La solution la moins acide : …
La solution la plus basique : …
4- Classer les solutions basiques de plus basique au moins basique (1Pt)
……………………………………………………………………………………….
5- On met une quantité de la solution « B » de pH=2,6 dans un volume d’eau
5-1- Comment appelle-t-on cette technique ? quel est son but ? (0,5Pt)
……………………………………………………………………………………….
5-2- Parmi les valeurs suivantes, entourer la valeur de pH de la solution obtenue (0,5Pt)
pH= 7
pH= 3,5
pH= 1,3
pH= 12
Partie B : la combustion PVC (sa formule est : C₂H₃Cl)
Combustion dans le dioxygène de l’air produit : la vapeur d’eau, le dioxyde de carbone, le carbone et chlorure d’hydrogène.
Application
- – Entonnoir
- – Gouttelettes d’eau
- – Trompe à eau
- – Flacon
- – Eau de chaux troublée
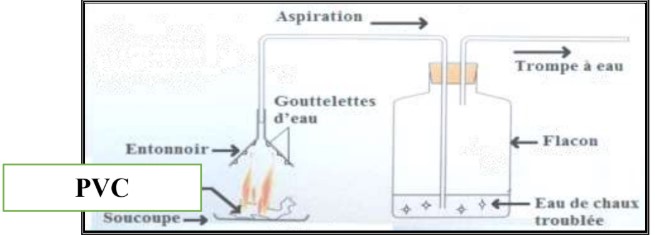
1) Citer les noms des réactifs et les produits de cette réaction (1Pt)
a- Les réactifs : ……………………
b- Les produits : ……………………
2) Écrire le bilan de cette réaction (1Pt)
……………………………………………………………………..
3) Quels sont les atomes entrant dans la composition de PVC ? (0,5Pt)
……………………………………………………………………..
4) Le PVC est une matière organique ? justifier votre réponse (1Pt)
……………………………………………………………………..
5) Préciser deux dangers de combustion de ces types de matériaux organiques
……………………………………………………………………..
Exercice 3: (3,5Pts)
- ➢ L’oxyde de fer III est le principal constituant de la rouille, c’est un corps solide poreux, par contre l’alumine est un corps non poreux
- ➢ Les atomes de fer ou d’aluminium, une fois en contact avec le dioxygène réagissent pour donner l’oxyde de chaque métal.
1. Écrire les équations chimiques équilibrées, qui produisent les oxydes cités. (1,5Pts)
……………………………………………………………………..
……………………………………………………………………..
2. On observe que, plus le temps passe plus le fer se transforme en rouille, par contre l’aluminium se couvre seulement d’une couche fine grise sans être corrodé. Donner une explication à ces observations. (1Pt)
……………………………………………………………………..
3. En déduire une méthode pour protéger le fer contre la rouille. (1Pt)
……………………………………………………………………..
Devoirs Corrigés Physique N°2 S1 3AC
