Devoirs Corrigés Physique N°3 S1 3AC
Modèle $N°1$
EXERCICE N°1 : (8 pts)
1. Répond par vrai ou faux : (2 pts)
a. Formule ionique d’hydroxyde de sodium est \( \text{Na}^+ + \text{HO}^- \) …
b. Formule ionique d’acide chlorhydrique est : \( \text{H}^+ + \text{Cl}^- \) …
c. Hydroxyde de sodium réagit avec les métaux : aluminium et zinc …
d. Hydroxyde de cuivre II précipité de couleur vert de formule chimique Cu (OH)₂ …
2. Compléter les phrases par les mots suivants : / nitrate d’argent/ dihydrogène /aluminium/zinc/cuivre / \(\text{Cu}^{2+}\) (3 pts)
a. Formule ionique de solution de ………… est \( \left( Ag^+ + NO_3^- \right) \)
b. précipité de couleur bleu confirme la présence des ions de …………
c. le gaz du ………… de formule chimique \( H_2 \) il brûle lorsqu’on présente une allumette enflammée à l’extrémité du tube.
d. l’acide chlorhydrique réagit avec les métaux : … et …
e. hydroxyde de sodium ne réagit pas avec les métaux …………
3. Coche la bonne réponse : (1,5 pts)
a. L’acide chlorhydrique ne réagit pas avec le métal :
cuivre
fer
zinc
b. Hydroxyde de sodium réagit avec le métal :
zinc
cuivre
fer
c. Formule chimique de précipité d’hydroxyde de cuivre II :
Cu (OH)₂
Zn (OH)₂
Fe (OH)₂
4. Compléter le tableau : (1,5 pts)
| ion | Formule chimique |
|---|---|
| … | \( Na^+ \) |
| chlorure | … |
| De fer II | … |
EXERCICE N°2 : (8 pts)
Ahmed a versé des gouttes de solution d’acide chlorhydrique dans un tube à essai contenant le zinc et a observé un dégagement de gaz et une solution A :
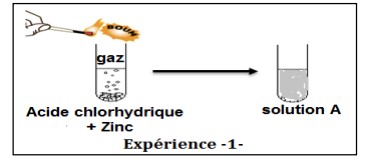
1. Donner la formule ionique chimique de la solution d’acide chlorhydrique ……………………(1 pt)
2. Quel est le nom du gaz produit : ………… sa Formule : … (1 pt)
Ahmed mis la solution obtenus dans l’experience -1- dans deux tubes à essais 1 et 2. Il a effectué les exépriences suivantes:
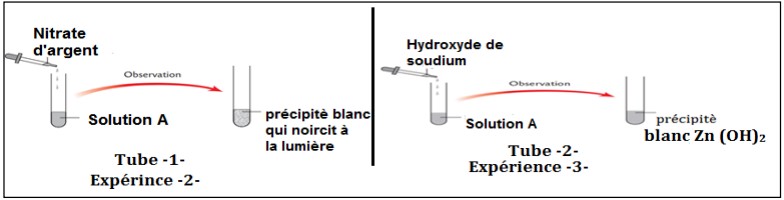
1. Quels ions ont été identifiés dans le Tube 1 (l’expérience -2-) ? …………………… (0,5 pt)
2. Écrire l’équation de précipitation dans tube -1- (l’expérience -2-) ………………………………………………………. (1 pt)
3. Quels ions ont été identifiés dans tube 2 (l’expérience -3-) ? …………………… (0,5 pt)
4. Donner le nom de précipité blanc Zn(OH)₂ : …………………… (1 pt)
5. Écrire l’équation de précipitation dans tube -2- (l’expérience -3-) ………………………………………………………. (1 pt)
6. Écrire l’équation bilan de la réaction du zinc avec l’acide chlorhydrique (l’expérience -1-) ………………………………………………………. (1 pt)
7. Écrire l’équation simplifiée de la réaction du zinc avec l’acide chlorhydrique (l’expérience -1-) ………………………………………………………. (1 pt)
EXERCICE N°3 : (4 pts)
Pour savoir le nom d’une solution Y on a réalisé deux expériences :
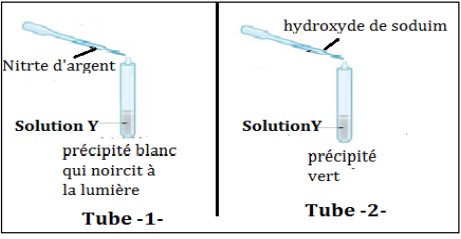
1. Pour tube -1-
a. Préciser le nom d’ion identifié dans tube -1- : …………………… (0,5 pt)
b. Écris l’équation de la précipitation : ………………………………………………………. (1 pt)
2. Pour tube -2-
a. Préciser le nom d’ion identifié dans tube -2- : …………………… (0,5 pt)
b. Le nom du précipité vert : …………………… (0,5 pt)
c. Écrire l’équation de la précipitation : ………………………………………………………. (1 pt)
3. Ecrire la formule ionique (chimique) de la solution Y : …………………… (0,5 pt)
Modèle $N°2$
EXERCICE N°1 : (7 pts)
Situation expérimentale réalisée
1. Complétez les phrases par les mots qui convient : (3 pts)
Hydroxyde de sodium – électrons – positive – noyau – nitrate d’argent – nuage électronique
- L’atome est constitué d’un …………………… entouré d’…………………… formant un ……………………
- Le noyau d’un atome porte une charge électrique ……………………
- On prouve la présence des ions chlorure Cl⁻ par la solution ……………………
- Pour prouver la présence d’ion positif Zn²⁺ on ajoute ……………………
2. Répondez par vrai ou faux : (2 pts)
| Un matériau organique contient toujours des atomes d’oxygène et d’hydrogène | …. |
| Les solutions acides contiennent des ions d’hydrogène H⁺ en excès | …. |
| La solution de soude (Na⁺+OH⁻) réagit avec le zinc et l’aluminium | …. |
| Lorsqu’un atome perd un électron ou plus devient un anion | …. |
3. Reliez par des flèches entre les éléments suivants : (2 pts)
| rouille | • | • (Ag⁺, NO₃⁻) |
| Hydroxyde de cuivre | • | • (Al³⁺ + SO₄²⁻) |
| Solution de nitrate d’argent | • | • Fe₂O₃ |
| Sulfate d’Aluminium | • | • Cu(OH)₂ |
EXERCICE N°2 : (9 pts)
On considère le tableau suivant :
| Solution | lait | Eau | Hydroxyde de sodium | Acide chlorhydrique |
|---|---|---|---|---|
| Valeur du pH | 6.8 | 7.0 | 13.2 | 1.3 |
1. Type de solution (1 pt)
Classer les solutions dans le tableau en solution acide, basique, neutre :
……………………………………………………….
2. Réaction avec l’acide chlorhydrique (4,5 pts)
On ajoute un volume d’une solution d’acide chlorhydrique dans un tube à essai contenant du fer en poudre, on observe qu’il y a un dégagement d’un gaz (inodore et incolore), et disparition d’une partie de fer.
- a. Donnez la formule ionique de la solution d’acide chlorhydrique : ……………………
- b. Quel est le nom du gaz produit : …………………… Sa formule : ….
- c. Comment détecter ce gaz ? ……………………
- d. Quels sont les ions formés ? ……………………
- e. Écrire l’équation simplifiée de la réaction de fer avec la solution d’acide chlorhydrique : ……………………………………………………….
3. Précipitation avec l’hydroxyde de sodium (3,5 pts)
On ajoute une solution d’hydroxyde de sodium à la solution précédente contenant les ions de Fer, et on observe la formation d’une précipitation verte.
- Donnez le nom et la formule chimique du précipité obtenu :
- Le nom : ……………………
- La formule chimique : ……………………
- Écrire l’équation de cette précipitation : ……………………………………………………….
EXERCICE N°3 : (4 pts)
Basma et son amie ont trouvé au laboratoire une solution aqueuse (S) dans un flacon en plastique sans étiquette. Pour déterminer le nom et la formule chimique de cette solution (S), ils ont effectué les expériences suivantes :
- Expérience 1 : on ajoute une solution d’hydroxyde de sodium à la solution (S) et a obtenu un précipité bleu.
- Expérience 2 : on ajoute une solution de nitrate d’argent à la solution (S) et a obtenu un précipité blanc qui noircit avec la lumière.
1. Analyse de l’expérience 1 (1,5 pts)
Quel est l’ion qui a été identifié dans l’expérience 1 ? ……………………
Écrire l’équation de cette précipitation : ……………………………………………………….
2. Analyse de l’expérience 2 (1,5 pts)
Quel est l’ion qui a été identifié dans l’expérience 2 ? ……………………
Écrire l’équation de cette précipitation : ……………………………………………………….
3. Conclusion (1 pt)
Déduire le nom et la formule ionique de cette solution (S) :
Nom : ……………………
Formule ionique : ……………………
Modèle $N°3$
Exercice 1: (8 points)
1- Répondre par Vrai ou Faux (2.5 pts)
| Le fer réagit avec l’acide chlorhydrique | |
| Hydroxyde de zinc est un précipité bleu | |
| Le cuivre réagit avec la soude | |
| La formule chimique de la soude (Na+ + HO–) |
2- Compléter les phrases suivantes : (fer – cuivre – nitrate d’argent – aluminium – zinc)
a) La solution d’acide chlorhydrique réagit avec et et le mais ne réagit pas avec .
b) La solution d’hydroxyde de sodium réagit avec et mais ne réagit pas avec et .
c) On prouve la présence des ions chlorure Cl– par la solution .
3- Relie par une flèche
| Cu2+ + SO42- | • | sulfate de cuivre |
| Fe2+ + SO42- | • | chlorure de fer III |
| Fe3+ + 3Cl– | • | sulfate de fer II |
| Zn2+ + 2Cl– | • | chlorure de zinc |
Exercice 2 : Identification de solution
Pour savoir le nom d’une solution Y on a réalisé deux expériences :
Expérience 1 :
On met un peu de la solution Y dans un tube puis on verse des gouttes d’hydroxyde de sodium (Na++OH–), on obtient un précipité bleu
- Préciser le nom d’ion identifié :
- Le nom du précipité : Sa formule :
- Écrire l’équation de la précipitation :
Expérience 2 :
On met une quantité de la solution Y dans un autre tube puis on verse quelques gouttes de Nitrate d’argent (Ag++NO3–), on obtient un précipité blanc qui noircit à la lumière.
- Préciser le nom d’ion identifié :
- Le nom du précipité : Sa formule :
- Écrire l’équation de la précipitation :
- Conclure la formule ionique de la solution Y :
- Déduire alors le nom de cette solution :
Exercice 3 : Identification d’un métal
On met des morceaux d’un métal X inconnu dans un tube à essai contenant de l’acide chlorhydrique, à un échantillon de la solution obtenue nous ajoutons des gouttes de solution d’hydroxyde de sodium et on observe la formation d’un précipité blanc.
- Quel est le nom du précipité blanc ?
- Quelle est sa formule chimique ?
- Écrire le symbole et le nom de l’ion détecté :
- Écrire la réaction de précipitation :
- Déduire le nom du métal X utilisé ? Justifier votre réponse :
- Écrire l’équation bilan et simplifiée de la réaction du métal X avec l’acide chlorhydrique :
Modèle $N°4$
Exercice 1: (8 pts)
1) Répondez par « Vrai » ou « faux » : (2,5 pts)
| Le cuivre réagit avec l’acide chlorhydrique | |
| La formule chimique de la solution chlorure d’hydrogène est HCl | |
| Hydroxyde de cuivre II est un précipité vert | |
| L’équation réduite (simplifiée) de réaction de l’acide chlorhydrique avec le zinc est : 2H+ + Zn2+ → H2 + Zn | |
| Pour identifier l’ion zinc on ajoute quelques gouttes d’hydroxyde de sodium |
2) Relie chaque espèce chimique à certaines de ses propriétés : (2,5 pts)
| Espèce chimique | Certaines de ses propriétés |
|---|---|
| Na+ + OH– | • Blanc noircit a l’abri de la lumiére |
| AgCl | • La soude : solution basique |
| Al3+ | • Donne un précipité bleu avec une solution de soude |
| Cu2+ | • Donne un précipité gélatineux blanc avec une solution de soude |
| Zn2+ | • Ion non métallique |
| Cl– | • Donne un précipité blanc avec une solution de soude |
3) Compléter les phrases : (3 pts)
a. L’acide chlorhydrique réagit avec les métaux : …………. et …………. et …………. le mais ne réagit pas avec ………….
b. Hydroxyde de sodium réagit avec les métaux : …………. et …………. et ne réagit pas avec les métaux …………. et ………….
Exercice 2 : (8 pts)
Sur une quantité de poudre de fer, on lui ajoute quelques gouttes d’acide chlorhydrique, on observe : un dégagement d’un gaz qui produit une détonation avec la flamme.
- Donner la formule chimique d’acide chlorhydrique : (1 pts)
- Écrire l’équation bilan de cette réaction chimique : (1,5 pts)
- Donner le nom du gaz dégagé et comment on peut le détecter : (1,5 pts)
- Si on considère que cette réaction produit 160 cm3 de dihydrogène :
- Donner la relation entre la masse volumique (ρ), la masse (m) et le volume (V) :(1 pts)
- Calculer la masse de dihydrogène produit :(1,5 pts)
On donne la masse volumique de H2 : ρ(H2 )= 0,08 g/L
- Donnez quelques précautions à prendre lors de l’utilisation de solutions concentrées (3) :(1,5 pts)
- …………
- …………
- …………
Exercice 3 (4 pts)
On met dans deux tubes deux échantillons d’une même solution aqueuse incolore X et on effectue les tests d’identification des ions suivants :
- On ajoute au premier tube 1 : des gouttes de nitrate d’argent et on remarque la formation d’un précipité blanc qui noircit en présence de la lumière.
- On ajoute dans le deuxième tube 2 : des gouttes de solution d’hydroxyde de sodium (la soude) et on remarque la formation d’un précipité vert.
1) Remplissez le tableau suivant : (2,5 pts)
| Nom du précipité obtenu | Equation de précipitation | Formule et nom de l’ion détecté | |
|---|---|---|---|
| Test d’identification 1 | |||
| Test d’identification 2 |
2) En déduire le nom et la formule de la solution aqueuse X : (1,5 pts)
Nom :
Formule :
Devoirs Corrigés Physique N°3 S1 3AC
