Examens locaux corrigés Physique 3AC مادة الفيزياء والكيمياء الإمتحان المحلي الموحد
01 النموذج
الإمتحان المحلي الموحد
لنيل شهادة السلك الإعدادي
دورة يناير
مادة الفيزياء والكيمياء – المعامل 1
مدة الإنجاز: 1 ساعة
Exercice 01: Testez vos informations
1
Compléter les phrases par les mots suivants :
(nuage ; gagné ; noyau ; perdu ; matière organique-carbone)
Une est constituée essentiellement des atomes d’hydrogène et de.
Un ion est un atome qui a ou un ou plusieurs électrons.
L’atome est constitué d’un entouré d’électrons formant un électronique.
2
Répondre par Vrai ou Faux :
Lorsqu’on dilue une solution basique, son pH augmente
Vrai
Faux
Le fer : caractérisé par son attraction par les aimants
Vrai
Faux
La formule chimique de la rouille est Fe₂O₃
Vrai
Faux
3
Cocher la bonne réponse :
A- La charge des électrons d’un atome est:
Qe = +Ze
Qe = -Ze
Qe = 0e
B- La réaction chimique entre l’acide chlorhydrique et le Zinc est modélisée par l’équation :
Zn + 2H+ ⟶ H₂ + Zn2+
2Zn + 2H+ ⟶ H₂ + Zn2+
4Zn + 2H+ ⟶ H₂ + 3Zn2+
C- Le pictogramme qui indique que la solution est inflammable (قابل للاشتعال) est:
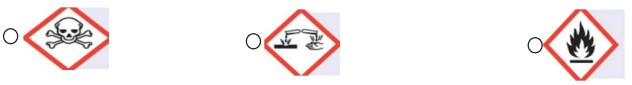
4
Classer les éléments suivants en objets et matériaux :
Livre ; Bois ; Chaise ; Verre ; Téléphone ; Fer ; Table ; Zinc
Exercice 02: Appliquez vos informations
الجزء 1
Partie 1 : On considère les solutions suivantes
| Solution | A | B | C | D | E | F |
|---|---|---|---|---|---|---|
| pH | 1.3 | 9.4 | 7 | 13 | 6.4 | 4.5 |
| Type de la solution |
1
Avec quel moyen on a mesuré le pH de ces solutions? Justifier votre réponse?
2
Classer les solutions dans le tableau en solution (acide, basique ou neutre)?
3
Identifier la solution plus acide et plus basique :
Solution plus acide :
Solution plus basique :
4
On ajoute la solution D de pH=13 à l’eau distillée
La valeur de pH après cette technique est égale :
pH = 14
pH = 13
pH = 8.5
الجزء 2
Partie 2 : L’atome du calcium (Ca) de numéro atomique Z=20
L’atome du calcium (Ca) de numéro atomique Z=20 perd 2 électrons pour devenir un ion.
1
Déterminer en fonction de ‘e’ la charge qe des électrons du calcium
2
Déterminer en fonction de ‘e’ la charge qn du noyau de cet atome
3
Déterminer en fonction de ‘e’ la charge qe des électrons de l’ion du calcium
4
Calculer la charge qion de l’ion du calcium en fonction de ‘e’
5
Écrire la formule de l’ion
الجزء 3
Partie 3 : Réaction acide chlorhydrique avec le fer
On ajoute une quantité de l’acide chlorhydrique dans un tube à essai contenant fer en poudre, on observe un dégagement gazeux qui produit une détonation lorsqu’on approche une flamme de l’orifice du tube à essai.
1
Donner le nom et la formule chimique du gaz dégagé
Nom du gaz :
Formule chimique :
2
Écrire l’équation simplifiée de la réaction d’acide chlorhydrique avec le fer
Exercice 03: Situation problème
Énoncé du problème :
Lorsque vous marchez devant un atelier de réparation de voitures, votre ami est surpris par un cadre (le cadre est en fer) de voiture rouillé alors que les jantes ne sont pas. Vous intervenez pour expliquer ce phénomène.

1
Donner deux facteurs favorisant ce phénomène
2
Donner le nom du composé essentiel de la rouille et sa formule chimique
Nom du composé :
Formule chimique :
3
Écrire l’équation chimique équilibrée de cette réaction
4
Proposer deux solutions pour protéger ces barreaux de la corrosion (التأكل)
02 النموذج
الإمتحان المحلي الموحد
لنيل شهادة السلك الإعدادي
دورة يناير
مادة الفيزياء والكيمياء – المعامل 1
مدة الإنجاز: 1 ساعة
Compléter, Joindre et Choisir
1
Compléter le texte par des mots clés (14×0.25Pt)
– Les matériaux sont classés en trois grandes familles : Les ………….., les ………….. et les ………….., ces derniers sont de bons ………….. d’électricité et de chaleur.
– L’atome est formé d’un ………….. central chargé ………….. autour duquel gravitent des ………….. chargés ……………
– Le nombre de charges positives d’un atome s’appelle ………….. il est noté ……………
– L’ion ………….. de symbole ………….. est responsable du caractère acide d’une solution.
– L’ion ………….. de symbole ………….. est responsable du caractère basique d’une solution.
2
Joindre correctement en précisant les bons couples (1.5Pt)
Exemple: (6 ; f)
(….. ; a) ; (….. ; b) ; (….. ; c) ; (….. ; d) ; (….. ; f)
Colonne 1
1. Hydroxyde de fer II
2. Hydroxyde de cuivre II
3. Chlorure de fer III
4. Hydroxyde de potassium
5. Nitrate d’argent
Colonne 2
a. (Ag+ + NO3–)
b. Fe(OH)2
c. (K+ + HO–)
d. Cu(OH)2
e. (Fe3+ + 3Cl–)
3
Entourer la bonne réponse (7×0.25Pt)
– Les anions/cations proviennent d’atomes ou groupes d’atomes ayant gagné des électrons, dans ce cas ils sont chargés positivement / négativement.
anions
cations
positivement
négativement
– Les anions/cations proviennent d’atomes ou groupes d’atomes ayant perdus des électrons, dans ce cas ils sont chargés positivement / négativement.
anions
cations
positivement
négativement
– La solution de chlorure d’hydrogène a pour formule :
(H+ + Cl–)
HCl2
HCl
– Le lait est faiblement acide son pH est :
pH = 1,2
pH = 3,2
pH = 6,2
– La solution de soude est fortement basique son pH est :
pH = 10
pH = 8
pH = 13
4
Mesure du pH de solutions
On mesure les valeurs du pH de quelques solutions à l’aide d’un pH-mètre, on note les résultats dans le tableau suivant :
| Solutions | A | B | C | D |
|---|---|---|---|---|
| Valeur | 1.2 | 7.0 | 13.2 | 6.8 |
| Caractère |
a) Préciser les caractères des solutions dans le tableau ci-dessus. (1Pt)
b) On ajoute 990mL d’eau distillée à 10mL de la solution A et on ajoute 990mL d’eau distillée à 10mL de la solution C. (0.5Pt)
– Comment appelle-t-on cette opération ?
c) Comment évoluera le pH de chacune de ces deux solutions après cette opération. (0.5Pt)
– Le pH de la solution A :
– Le pH de la solution C :
Identification d’ions et Tests chimiques
Salma a trouvé dans le laboratoire une solution de couleur rouille, placée dans un flacon, elle a supposé qu’il s’agisse d’une solution de chlorure de fer III (Fe3+ + 3Cl–). Pour vérifier que cette solution contient bien les ions Fe3+ et Cl–. Aider Salma à répondre aux questions suivantes :
1
Solutions d’identification (1Pt)
– Quelles solutions doit utiliser Salma pour identifier ces ions dans la solution ?
– La solution utilisée pour identifier la présence de Fe3+ est :
– La solution utilisée pour identifier la présence de Cl– est :
2
Tableau d’identification (1Pt)
| Ion identifié | Ion identifiant |
|---|---|
3
Couleur des précipités (1Pt)
– Donner la couleur de chaque précipité au cours des deux tests.
4
Équations de précipitation (1Pt)
– Écrire les équations de précipitations correspondantes à chacun des deux tests.
Réaction chimique : Zinc et Acide chlorhydrique
I
Atome de zinc (1.5Pt)
Le zinc, de numéro atomique Z=30, est un métal utilisé pour protéger le fer des oxydations.
– Quel est le nombre d’électrons de l’atome de zinc ? (0.5Pt)
– Donner la charge du noyau de l’atome de zinc en fonction de (e). (0.5Pt)
– Donner la charge des électrons de l’atome de zinc en fonction de (e). (0.5Pt)
II
Réaction avec l’acide chlorhydrique (2.5Pt)
Dans un tube à essai contenant 20mL d’acide chlorhydrique, on verse 1,2g de poudre de zinc, il se forme un gaz et des ions apparaissent dans la solution.
1) Quel est le nom du gaz formé, et quelle est sa formule ? (0.5Pt)
– Le nom du gaz :
– La formule du gaz :
2) Comment peut-on l’identifier ? (0.5Pt)
3) Quels sont les ions formés lors de cette réaction ? (0.5Pt)
4) Comment varie le pH de la solution au cours de cette réaction ? Justifier votre réponse (0.5Pt+0.5Pt)
5) Écrire l’équation bilan équilibrée de cette réaction. (0.5Pt)
6) Écrire l’équation simplifiée de cette réaction. (0.5Pt)
7) Lorsque le dégagement gazeux cesse, on mesure le pH de la solution, on trouve une valeur égale à 3,65. (0.5Pt+0.5Pt)
a) Reste-t-il de l’acide à la fin de l’expérience ? justifier votre réponse.
b) Pourquoi la réaction s’est-elle arrêtée ?
8) Comment peut-on mettre en évidence la présence des ions formés ? (1Pt)
– La solution d’identification :
– Les ions identifiants :
03 النموذج
الإمتحان المحلي الموحد
لنيل شهادة السلك الإعدادي
دورة يناير
مادة الفيزياء والكيمياء – المعامل 1
مدة الإنجاز: 1 ساعة
Compléter, Vrai ou Faux, Relier et Choisir
1
Compléter les phrases ci-dessous (3 points)
Les ions responsables de l’acidité sont ……………… tandis que celles qui sont responsables de la basicité sont ……………….
La matière organique est constituée essentiellement des atomes de ……………… et ……………….
L’oxydation de l’aluminium produit ……………… de formule chimique ……………….
L’atome est électriquement neutre car ……………… est nulle.
Les grandes familles des matériaux sont ……………… et ……………… et ……………….
2
Répondre par vrai ou faux (2 points)
– Quand on dilue une solution basique, son pH augmente.
Vrai
Faux
– Un électron porte une charge électrique -e.
Vrai
Faux
– Le PE est essentiellement constitué d’atomes de carbone et oxygène.
Vrai
Faux
– La combustion des matières organiques produit essentiellement le CO₂ et H₂O.
Vrai
Faux
3
Relier par une flèche (2 points)
Colonne 1
CO
Al₂O₃
Le plastique
L’air humide
Colonne 2
Isolant électrique
Produit de la combustion incomplète
Alumine
Provoque la rouille de fer
Relier chaque élément de la colonne 1 à son correspondant dans la colonne 2
4
Choix multiple (1 point)
On dilue une solution aqueuse de pH = 4, le pH de la solution obtenue est :
pH = 7.5
pH = 6
pH = 12
Mesure du pH et Propriétés des Solutions
Le tableau suivant donne le pH de différentes solutions :
| Solution aqueuse | S1 | S2 | S3 | S4 | S5 |
|---|---|---|---|---|---|
| pH de la Solution | 1.1 | 8.7 | 13.6 | 4.5 | 7.0 |
| Nature de la Solution |
1
Nature des solutions (1 point)
Donner sur le tableau la nature de chaque solution.
2
Méthodes de mesure du pH (1 point)
Donner deux méthodes différentes qui permettent de mesurer le pH des solutions et préciser celle utilisée pour obtenir les mesures du tableau.
3
Solutions extrêmes (0.5 point)
Déterminer la solution la plus acide et la solution la moins basique.
Solution la plus acide :
Solution la moins basique :
4
Dilution de la solution S1 (1 point)
Ahmed veut diminuer la concentration et la dangerosité de la solution S1.
4-1. Quelle action peut-il faire pour rendre cette solution moins concentrée ? (0.5 point)
4-2. Comment évolue le pH de la solution lors de cette action ? (0.5 point)
5Formule de la solution S1 (0.5 point)
La solution S1 contient l’ion chlorure Cl⁻ et un autre ion. Déterminer la formule de cet ion et déduire la formule de la solution S1.
Formule de l’autre ion :
Formule de la solution S1 :
6
Sachant que le nombre d’électrons de l’ion de chlorure Cl⁻ est 18. (0.5 point)
6 -1- Déterminer le numéro atomique de l’atome du chlore Cl. (1 point)
6 -2- Calculer, en coulomb, la charge du noyau.. (1 point)
6 -3- Calculer en e, la charge des électrons de l’ion Cl⁻. (1 point)
Combustion de la Matière Organique
Expérience de combustion
La matière X est une matière organique ; Afin de comprendre les types d’atomes qui constituent la matière X, on réalise l’expérience ci-dessous :
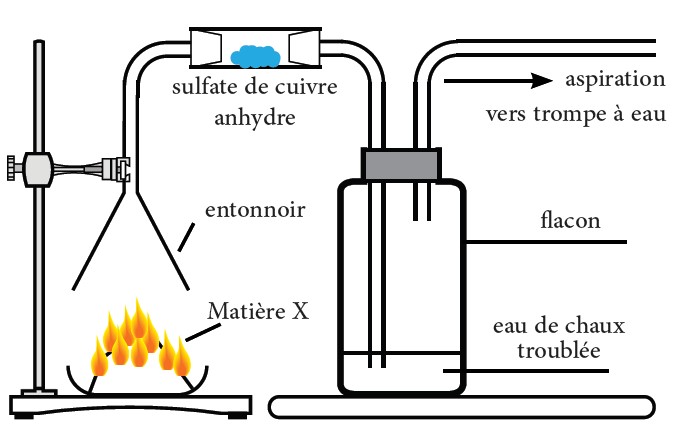
On observe que :
La combustion s’effectue avec une flamme jaune.
L’eau de chaux se trouble.
Formation de cyanure d’hydrogène HCN (Gaz toxique).
Le sulfate de cuivre (initialement blanc) devient bleu.
1
Type de combustion (1 point)
Quel est le type de cette combustion. Justifier votre réponse.
2
Produits de combustion (1 point)
Quels sont les produits de cette combustion ?
3
Réactifs de combustion (1 point)
Quels sont les réactifs de cette combustion ?
4
Atomes de la matière X (1 point)
Quelles sont les trois types d’atomes qui constituent la matière X ?
04 النموذج
الإمتحان المحلي الموحد
لنيل شهادة السلك الإعدادي
دورة يناير
مادة الفيزياء والكيمياء – المعامل 1
مدة الإنجاز: 1 ساعة
Compléter le texte et Répondre par Vrai ou Faux
1
Compléter le texte suivant par ce qui convient : (9×0.5pt)
– Le fil électrique est un corps se compose de …………….. qui est un matériau isolant, et de métal de cuivre, qui se distingue par sa couleur …………….. et c’est un matériau …………….. d’électricité.
– Un atome est constitué d’un ……………..
et …………….., et lorsqu’il perd ou gagne un ou plusieurs électrons, il se transforme en ………………
– L’air humide réagit avec l’aluminium et donne une couche de couleur …………….. appelée chimiquement ……………..sa formule chimique est ………………
2
Répondre par Vrai(V) ou Faux(F) : (4×0.5pt)
L’action de l’acide chlorhydrique sur le fer donne un gaz c’est le dioxygène. ……………..
Pour détecter l’ion de zinc, nous utilisons le chlorure de zinc. ……………..
Un cation est un atome qui a perdu un ou plusieurs électrons. ……………..
Le numéro atomique Z représente le nombre d’électrons d’un atome. ……………..
3
La combustion du plastique PVC
La combustion du plastique PVC dans l’air produit de l’eau (H2O) et un gaz qui fait troubler l’eau de chaux et du gaz chlorure d’hydrogène (HCl).
a) Quels sont les atomes constituant le plastique PVC ? (1pt)
b) À quel groupe de matériaux appartient le plastique PVC ? (0.5pt)
Réaction entre l’acide chlorhydrique et le zinc
Nous ajoutons une quantité de solution d’acide chlorhydrique du pH=1 dans un tube à essai avec la poudre du zinc Zn, et une réaction chimique se produit qui donne un gaz qui fait une petite détonation lorsqu’on approche une flamme de l’orifice du tube, et que le zinc métallique disparaît, puis une solution (S1) appelée chlorure de zinc du pH=7 se forme.
1
Formule ionique de l’acide chlorhydrique (0.5pt)
Écrire la formule ionique de l’acide chlorhydrique :
2
Nature des solutions (1pt)
Déterminer la nature des solutions et justifier votre réponse :
– Acide chlorhydrique : …………….. parce que :……………..
– Chlorure de zinc : ……………..parce que :
3
Nom et formule du gaz (1pt)
Quel est le nom du gaz produit et quelle est sa formule ?
4
Équation de la réaction (1pt)
Écrivez l’équation de la réaction simplifié entre l’acide chlorhydrique et le zinc :
5
Dilution de l’acide chlorhydrique (1pt)
– Si nous diluons la solution d’acide chlorhydrique, comment le pH change-t-il ? (0.5pt)
6
la valeur du pH de solution obtenue lors de la dilution (0.5pt)
– Si vous savez que la valeur du pH de l’acide chlorhydrique augmente d’une unité (1) quand on le dilue 10 fois. Calculer la valeur du pH de solution obtenue lors de la dilution on ajoutant 990 ml d’eau à 10 cm3 de solution d’acide chlorhydrique (pH=1).
7
Tableau des ions du zinc (2pt)
Le numéro atomique du zinc est Z = 30. Complétez le tableau ci-dessous, où (e) est la charge élémentaire.
| Symbole d’ion | Nombre d’électrons d’ion | Charge d’ion | Charge d’électrons d’atome | Charge de noyau d’ion |
|---|---|---|---|---|
| +2e |
8
Détection de l’ion du zinc (1.5pt)
Pour détecter l’ion du zinc dans la solution (S1), nous ajoutons une solution d’hydroxyde de sodium à cette dernière, et un précipité blanc se forme.
a) Quel est le nom du précipité et quelle est sa formule (0.5pt) ?
b) Quel est le nom et la formule de l’ion détecteur (0.5pt) ?
c) Écrire l’équation de précipitation correspondante (0.5pt) ?
Discussion sur la corrosion du fer et de l’aluminium
Tu assisté à la discussion suivante au sein d’un groupe de vos amis :
– Mohammed : Pourquoi la porte de notre maison en fer rouille-t-elle et se détruit-t-elle plus sur sa face inférieure que sur sa partie supérieure, contrairement aux fenêtres en aluminium ?
– Khadija : Parce que le fer réagit avec l’air, contrairement à l’aluminium.
Sur la base de ce que vous avez étudié, essayez de donner votre avis sur ce que vos collègues ont dit, en utilisant les questions suivantes :
1
Rouille du fer (2pt)
Expliquez la cause de la rouille du fer avec l’écriture de l’équation de la réaction chimique.
2
Opinion de Khadija sur l’aluminium (2pt)
Expliquez est ce que l’opinion de Khadija est juste ou non concernant l’aluminium, en la justifiant par une équation chimique.
05 النموذج
الإمتحان المحلي الموحد
لنيل شهادة السلك الإعدادي
دورة يناير
مادة الفيزياء والكيمياء – المعامل 1
مدة الإنجاز: 1 ساعة
Compléter, Classer et Répondre
1
Complétez les phrases ci-dessous (2.5 points)
– Les ions responsables de l’acidité sont …………….. tandis que celles qui sont responsables de la basicité sont …………….. .
– Les matières organiques sont constituées essentiellement des atomes de …………….. et atomes de …………….. .
– L’on provient d’un seul atome est appelé ion …………….. .
Mots à utiliser : Monoatomique ; Carbone ; H+ ; hydrogène ; OH–
2
Classez les mots suivants selon le tableau (2.5 points)
Mots à classer : Tricot – fer – voiture – plomb – plastique – crayon – bois – papier cartonné – Or – PVC
| Corps | Matériaux | |
|---|---|---|
| Organiques | Métaux | |
3
Répondez par Vrai ou Faux (1.5 points)
– Un anion porte une charge positive ……
Vrai
Faux
– Le PE flotte dans l’eau douce ……
Vrai
Faux
– Lorsqu’on dilue une solution acide, son pH diminue ……
Vrai
Faux
4
Complétez le tableau ci-dessous (1.5 points)
| Solution | A | B | C | D | E | F |
|---|---|---|---|---|---|---|
| pH | 10 | 2 | 4.5 | 7 | 9 | 11.5 |
| Nature |
L’Aluminium : Propriétés et Réactions
L’aluminium Al est l’un des métaux les plus utilisés dans l’emballage et dans l’industrie.
1
Déterminez le numéro atomique Z d’aluminium (1 point)
Sachant que son noyau porte une charge positive : Qn = + 20,8×10-19 C.
2
Déduisez la charge électrique des électrons d’atome d’Al (1 point)
3
L’ion aluminium (2 points)
Sachant que l’atome d’aluminium perd trois électrons pour se transformer en ion d’aluminium :
3-1. Donnez le symbole de l’ion d’aluminium :
3-2. Calculez en coulomb (C), la charge des électrons de l’ion d’aluminium, on donne e = 1,6×10-19 C :
3-3. Déterminez en coulomb (C), la charge de l’ion aluminium, on donne e = 1,6×10-19 C :
4
Oxydation de l’aluminium (4 points)
Au contact avec l’air humide, l’aluminium s’oxyde et forme une couche fine appelée Alumine.
4-1. Donnez la formule chimique de l’alumine : (1 point)
4-2. Écrivez l’équation chimique de la formation d’alumine : (1 point)
4-3. Proposez une technique pour protéger l’aluminium : (1.5 points)
Sulfate de fer et Tests d’identification
Le sulfate de fer vendu dans les commerces se présente sous forme d’une poudre verte. Il est utilisé pour traiter les gazons. Après avoir ouvert un paquet neuf, Salim dissout un peu de poudre dans l’eau, il prélève une partie de solution et y ajoute quelques gouttes d’hydroxyde de sodium. Il observe un précipité.
1) Quelle est la couleur du précipité observé par Salim, ainsi que sa formule ? (1 point)
– La couleur :
– La formule :
2) Écrivez l’équation chimique de la précipitation : (1 point)
Salim laisse la solution à l’air libre et revient quelques jours plus tard. Il prélève à nouveau un peu de solution et y ajoute quelques gouttes de soude, il observe alors un précipité de couleur rouille.
3-1) Quel ion a-t-il mis en évidence lors du 2ème ajout de soude ? (0.5 point)
3-2) Écrivez la formule chimique du précipité de couleur rouille : (0.5 point)
3-3) Quelle transformation ont subi les ions Fe2+ après quelques jours passés à l’air libre ? (1 point)
Examens locaux corrigés Physique 3AC مادة الفيزياء والكيمياء الإمتحان المحلي الموحد
