La dissolution dans l’eau exercices corrigés
La dissolution dans l’eau
I. Notion de la solution aqueuse.
1. Activité expérimentale:
On ajoute une quantité de sel dans un tube à essai contenant de l’eau, puis on réalise la même expérience en utilisant le sable.

2. Observation:
– Après l’agitation le sel disparu totalement dans l’eau en formant de mélange homogène. On dit que le sel est soluble dans l’eau.
– Le sable ne se dissout pas dans l’eau, en formant un mélange hétérogène, on dit que le sable insoluble dans l’eau.
c. Conclusion:
– Le sel est un soluté, l’eau est un solvant, le mélange obtenu est une solution aqueuse.
– La solution aqueuse est un mélange homogène composée d’un solvant (l’eau) et d’un soluté.
II. Type des solutions aqueuses.
1. Activité expérimentale:
On verse différentes quantité de sel dans un tube à essai contenant 20 ml d’eau.
1. Observation:
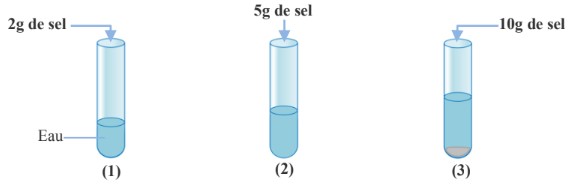
– La solution aqueuse (1) est moins saline que la solution aqueuse (2).
– Tube (3) : le sel ne se dissout plus dans l’eau.
3. Conclusion:
– La solution (1) est une solution diluée.
– La solution (2) est une solution concentrée.
– La solution (3) est une solution saturée.
Remarque:
– Les liquides et les gaz peuvent être dissous dans l’eau.
– Au cours de la dissolution la masse totale du solvant et du soluté ne change pas.
– La fusion et la dissolution sont deux transformations différentes.
III – La masse totale est elle conservée lors d’une dissolution ?
1. Expérience :
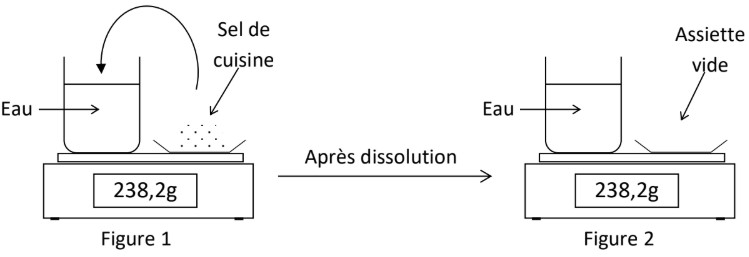
2. Conclusion :
La masse totale du solvant et du soluté ne change pas au cours de la dissolution.
Exercice 1:
Compléter par les mots suivants: mélange – solvant – soluté – hétérogène – dissolution -solution – homogène -ne change pas – pur.
$1)$ Au cours d’une $……………$ une substance appelée le $……………$ est dissoute dans un $……………$ le résultat est une $……………$ Le $……………$ peut être un solide, un liquide ou un gaz.
$2)$ La $……………$ contient plus d’une substance alors qu’un corps $……………$ n’en contient qu’une seule.
$3)$ Dans un mélange $……………$, les constituants ne peuvent être distingués à l’œil nu contrairement à un mélange $……………$
$4)$ Lors de la fusion de la glace, sa masse $……………$
$1)$ Au cours d’une dissolution, une substance appelée le soluté est dissoute dans un solvant, le résultat est une solution. Le soluté peut être un solide, un liquide ou un gaz.
$2)$La solution contient plus d’une substance alors qu’un corps pur n’en contient qu’une seule.
$3)$Dans un mélange homogène, les constituants ne peuvent être distingués à l’œil nu contrairement à un mélange hétérogène.
$4)$ Lors de la fusion de la glace, sa masse ne change pas.
Exercice 2:
Réponds par Vrai ou par Faux
– Dans une solution d’eau salée, le sel est le solvant $…………$
– Dans une solution d’eau salée, l’eau est le soluté .$………..$
– La masse du solvant ajoutée à la masse du soluté est égale à la masse de la solution. $…………$
– Le sable est insoluble dans l’eau $…………$
Exercice 3:
On prépare trois solutions de même volume d’eau en y faisant dissoudre différentes quantités de sucre :
Nommer chaque solution ?
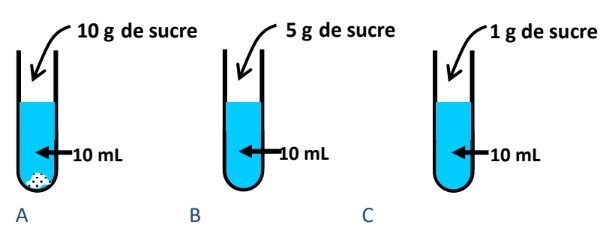
Solution $A$ : ………………………………………………………………………………
Solution $B$ : ………………………………………………………………………………
Solution $C$ : ………………………………………………………………………………
Exercice 4:
Expliquer pourquoi il y a une différence entre la dissolution et la fusion ?
Exercice 5:
Cocher la bonne réponse
| Matière | Soluble dans l’eau | Insoluble dans l’eau | Mélange homogène | Mélange hétérogène |
|---|---|---|---|---|
| Sel | ||||
| Beurre | ||||
| Fer | ||||
| Essence | ||||
| Air | ||||
| Vinaigre | ||||
| Alcool |
Exercice 6:
On prépare trois solutions de même volume $(10 ml)$ d’eau en faisant dissoudre différentes quantités de sucre, sachant que la solubilité de sucre dans l’eau est $2000 g/L$.
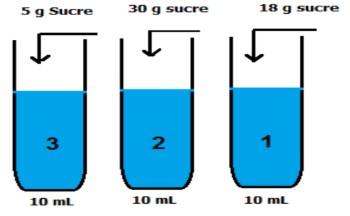
$1)$ Calculer la masse maximale de sucre qu’on peut dissoudre dans $10 ml$ d’eau.
$2)$ Nommer les solutions préparées.
– Solution (1) est $…………………………….$
car $………………………………$
– Solution (2) est $…………………………….$
car $……………………………………$
– Solution (3) est $…………………………….$
car $………………………….$
Exercice 7:
A partir de la figure ci-contre.
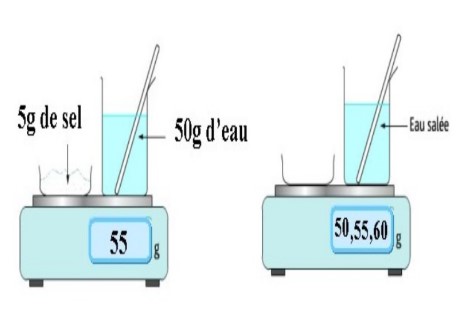
$1)$ Déterminer :
– Le solvant :
– Le soluté :
$2)$ Entourer la masse de la solution sur la balance.
Exercice 8:
On verse $30 ml$ d’eau dans un bécher de masse $120g$, puis on y ajoute $10g$ de sucre. Après agitation on obtient une solution homogène.
La solubilité du sucre dans l’eau à $20 °C$ est $2kg/L$ et la masse volumique de l’eau est $1kg/L$.
$1)$ Préciser le solvant et le soluté
$2)$ Est-ce que le sucre a disparu du bécher ?
$3)$ Si on pose le bécher sur une balancer électrique. Quelle valeur affichera-t-
elle ?
$4)$ Quelle est la masse minimale du sucre qu’il faut ajouter pour obtenir deux
phases ?
Exercice 9:
On dissout $200g$ du sel à $20°C$ dans un $800ml$. On rappelle que la solubilité du sel à sel à cette température est $360g/L$.
$1)$ Justifier pourquoi la solution n’est pas saturée.
$2)$ On fait bouillir le mélange puis on laisser froidir. Quel est le volume minimal de la quantité d’eau vaporisée pour avoir après refroidissement un mélange non homogène.
La dissolution dans l’eau exercices corrigés
