La géométrie de quelques molécules – exercices corrigés
Exercice 1 :
Règles du duet et de l’octet
Facile
Question 1.1
La règle du duet s’applique aux atomes ayant un numéro atomique Z :
Z ≤ 4
5 ≤ Z ≤ 18
Z ≥ 19
Tous les atomes
Question 1.2
Les gaz rares sont chimiquement stables car :
Leurs couches externes sont saturées
Ils n’ont pas d’électrons
Ils ont une charge positive
Ils sont très légers
Question 1.3
Un atome de fluor (Z=9) forme l’ion F⁻ pour :
Acquérir la structure électronique du néon
Perdre un électron
Acquérir la structure électronique de l’argon
Augmenter sa charge nucléaire
Question 1.4
La règle de l’octet stipule que les atomes tendent à avoir :
8 électrons sur leur couche externe
8 électrons au total
8 protons dans le noyau
8 neutrons dans le noyau
Question 1.5
Un atome de magnésium (Z=12) forme l’ion Mg²⁺ pour acquérir la structure électronique :
Du néon
De l’argon
Du krypton
De l’hélium
Règles du duet et de l’octet
Question 1.1 : La règle du duet s’applique aux atomes avec Z ≤ 4 (H, He, Li, Be) qui cherchent à acquérir 2 électrons sur leur couche externe, comme l’hélium.
Question 1.2 : Les gaz rares ont des couches externes saturées (duet pour He, octet pour les autres), ce qui explique leur stabilité chimique.
Question 1.3 : Le fluor (Z=9, structure: (K)²(L)⁷) gagne 1 électron pour former F⁻ et acquérir la structure du néon (K)²(L)⁸.
Question 1.4 : La règle de l’octet concerne spécifiquement le nombre d’électrons sur la couche externe (8 électrons).
Question 1.5 : Le magnésium (Z=12, structure: (K)²(L)⁸(M)²) perd 2 électrons pour former Mg²⁺ et acquérir la structure du néon.
Exercice 2 :
Représentation de Lewis
Moyen
Question 2.1
Dans la représentation de Lewis, une liaison covalente simple est représentée par :
Un trait simple (–)
Un double trait (=)
Un triple trait (≡)
Un point (•)
Question 2.2
Combien de doublets non liants possède la molécule d’eau (H₂O) dans sa représentation de Lewis ?
1
2
3
4
Question 2.3
Quelle molécule suivante possède une liaison triple dans sa représentation de Lewis ?
O₂
N₂
CO₂
CH₄
Question 2.4
Dans la molécule de méthane CH₄, l’atome de carbone forme :
4 liaisons simples
2 liaisons simples et 1 liaison double
1 liaison simple et 1 liaison triple
2 liaisons doubles
Question 2.5
Combien de doublets liants et non liants possède la molécule d’ammoniac NH₃ ?
3 liants, 1 non liant
2 liants, 2 non liants
4 liants, 0 non liant
1 liant, 3 non liants
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 3 :
Isomères et Géométrie Moléculaire
Difficile
Question 3.1
Des isomères sont des composés qui ont :
Même formule brute mais formules développées différentes
Même formule développée mais formules brutes différentes
Mêmes propriétés physiques et chimiques
Même géométrie mais atomes différents
Question 3.2
La géométrie de la molécule d’eau H₂O est :
Linéaire
Tétraédrique
Plane coudée (en V)
Pyramide à base triangulaire
Question 3.3
La géométrie de la molécule de méthane CH₄ est tétraédrique car :
L’atome de carbone a 4 domaines électroniques identiques
Les atomes d’hydrogène se repoussent fortement
La molécule est très symétrique
Le carbone a une grosse taille atomique
Question 3.4
La formule brute C₂H₆O correspond à deux isomères : l’éthanol et l’oxyde de diméthyle. Quelle affirmation est correcte ?
Ils ont les mêmes propriétés chimiques
Ils ont la même géométrie autour de l’atome d’oxygène
L’éthanol a un groupe OH alors que l’oxyde de diméthyle a un atome d’oxygène central
Ils ont le même point d’ébullition
Question 3.5
La géométrie de la molécule de dioxyde de carbone CO₂ est linéaire car :
L’atome de carbone n’a pas de doublet non liant
Les deux doubles liaisons C=O se repoussent symétriquement
La molécule est apolaire
Les atomes d’oxygène sont identiques
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 4:
Consigne : Cocher la (ou les) bonne(s) réponse(s) pour chaque question.
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 5: Atomes, ions et règle de duet et de l’octet
Consigne : Compléter le tableau suivant en appliquant les règles du duet et de l’octet.
| Atome | Z | Structure électronique de l’atome | Règle de duet ou de l’octet | Structure électronique de l’ion | Symbole de l’ion |
|---|---|---|---|---|---|
| Li | 3 | ||||
| O | 8 | ||||
| Ne | 10 | ||||
| Na | 11 | ||||
| Mg | 12 | ||||
| Cl | 17 | ||||
| N | 7 | ||||
| F | 9 | ||||
| Be | 4 | ||||
| Al | 13 |
Corrigé de l’Exercice 2
| Atome | Z | Structure électronique de l’atome | Règle de duet ou de l’octet | Structure électronique de l’ion | Symbole de l’ion |
|---|---|---|---|---|---|
| Li | 3 | (K)²(L)¹ | Duet | (K)² | Li⁺ |
| O | 8 | (K)²(L)⁶ | Octet | (K)²(L)⁸ | O²⁻ |
| Ne | 10 | (K)²(L)⁸ | Déjà stable | (K)²(L)⁸ | Ne (pas d’ion) |
| Na | 11 | (K)²(L)⁸(M)¹ | Octet | (K)²(L)⁸ | Na⁺ |
| Mg | 12 | (K)²(L)⁸(M)² | Octet | (K)²(L)⁸ | Mg²⁺ |
| Cl | 17 | (K)²(L)⁸(M)⁷ | Octet | (K)²(L)⁸(M)⁸ | Cl⁻ |
| N | 7 | (K)²(L)⁵ | Octet | (K)²(L)⁸ | N³⁻ |
| F | 9 | (K)²(L)⁷ | Octet | (K)²(L)⁸ | F⁻ |
| Be | 4 | (K)²(L)² | Duet | (K)² | Be²⁺ |
| Al | 13 | (K)²(L)⁸(M)³ | Octet | (K)²(L)⁸ | Al³⁺ |
Rappels des règles :
- Règle du duet : Pour Z ≤ 4, les atomes tendent à avoir 2 électrons sur leur couche externe (comme l’hélium)
- Règle de l’octet : Pour 5 ≤ Z ≤ 18, les atomes tendent à avoir 8 électrons sur leur couche externe
- Gaz rares : Les atomes comme Ne sont déjà stables et ne forment pas d’ions
- Formation des ions : Les métaux perdent des électrons (cations +), les non-métaux gagnent des électrons (anions -)
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 6 : Représentation de Lewis, représentation de CRAM
Énoncé : Le tétrachloréthane ou tétrachlorure de carbone est un composé chimique chloré de formule brute : CCl4.
1) Donner la structure électronique d’un atome de carbone 12C et celle d’un atome de chlore \({}_{17}Cl\) .
Carbone (12C) :
Chlore (17Cl) :
2) Déterminer le nombre d’électrons de la couche externe des atomes de carbone et de chlore (pc et pcl).
Carbone (pc) :
Chlore (pcl) :
3) Calculer NT le nombre d’électrons apportés par l’ensemble des couches externes des atomes de la molécule.
NT :
4) En déduire Nd le nombre de doublets de la molécule.
Nd :
5) Préciser NL le nombre de doublets liants de chaque atome (liaisons covalentes).
NL :
6) Préciser NnL le nombre de doublets non liants.
NnL :
7) Vérifier que Nd = NL + NnL
Vérification :
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 7: Représentation de Lewis et géométrie moléculaire
Consigne : Compléter le tableau suivant en déterminant les différentes caractéristiques des molécules et leurs représentations de Lewis.
| Molécule | Atomes | Structure électronique | p | NT | Nd | NL | NnL | Représentation de Lewis |
|---|---|---|---|---|---|---|---|---|
| H₂O | \({}_{1}H\) | |||||||
| \({}_{1}H\) | ||||||||
| \({}_{8}O\) | ||||||||
| CO₂ | \({}_{6}C\) | |||||||
| \({}_{8}O\) | ||||||||
| \({}_{8}O\) | ||||||||
| N₂ | \({}_{7}N\) | |||||||
| \({}_{7}N\) | ||||||||
| HCl | \({}_{1}H\) | |||||||
| \({}_{17}Cl\) | ||||||||
| NH₃ | \({}_{7}N\) | |||||||
| \({}_{1}H\) | ||||||||
| \({}_{1}H\) | ||||||||
| \({}_{1}H\) |
Légende :
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 8: La géométrie de la molécule SiH₃Cl
Contexte : Le chlorosilane SiH₃Cl est un gaz qui intervient dans la préparation du silicium très pur destiné à l’électronique. Les éléments silicium, hydrogène et chlore ont pour numéros atomiques respectifs 14, 1 et 17.
Données utiles :
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 9: Isomérie d’une molécule
Contexte : On considère la molécule avec la formule brute suivante : C₂H₆O.
Données utiles :
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 10: Formule développée et type de liaison covalente
Objectif : Écrire les formules développées et les schémas de Lewis pour différentes molécules organiques et inorganiques.
Partie A – Molécules à liaisons simples
Les molécules des composés ci-dessous ne comportent que des liaisons simples :
CH₄
C₂H₄
C₂H₄Cl₂O
Partie B – Molécules avec liaisons multiples
Mêmes questions pour les molécules ci-dessous sachant qu’elles comportent toutes une liaison double ou triple :
O₂
N₂
C₂H₂
HCN
C₄H₈
C₃H₄
C₃H₆O
Instructions :
- Pour chaque molécule, écrire la formule développée et le schéma de Lewis
- Indiquer le type de liaison (simple, double, triple) pour chaque liaison
- Préciser les doublets non liants sur les schémas de Lewis
- Vérifier que tous les atomes respectent la règle de l’octet (ou du duet pour H)
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 11: La géométrie d’une molécule organosiliciée
Contexte : On étudie une molécule constituée d’un atome de silicium ({}_{14}Si\) et quatre atomes de carbone ({}_{6}C\) et des atomes d’hydrogène ({}_{1}H\).
Données utiles :
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 12: La molécule d’Aminoacétonitrile
Contexte : Voici le modèle moléculaire de la molécule d’Aminoacétonitrile. Cette molécule est un précurseur de la glycine, le plus simple des acides aminés.
Modèle moléculaire de l’Aminoacétonitrile
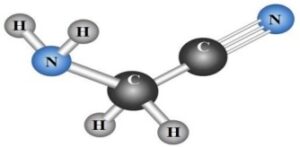
Informations sur l’Aminoacétonitrile :
- Précurseur de la glycine (acide aminé simple)
- Formule : NH₂-CH₂-C≡N
- Contient un groupe amine (-NH₂) et un groupe nitrile (-C≡N)
- Molécule importante en chimie prébiotique
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
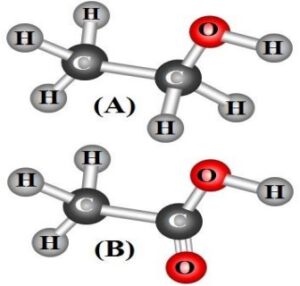
Exercice 13: L’éthanol et l’acide éthanoïque
Contexte : L’éthanol (A) est un alcool qui s’oxyde en acide éthanoïque (B) et qui est le principal constituant du vinaigre.
Éthanol (A) et Acide éthanoïque (B)

Éthanol :
Acide éthanoïque :
Éthanol :
Acide éthanoïque :
Éthanol :
Acide éthanoïque :
Éthanol :
Acide éthanoïque :
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
La géométrie de quelques molécules – exercices corrigés
