La chaleur et les changements d’état physique de la matière exercices corrigés
Le corps pur et ses caractéristiques
I. Le corps pur et ses caractéristiques:
1) Expérience :
On chauffe une quantité d’eau salée puis l’eau distillée et enfin la glace d’eau distillée. Lors du chauffage on enregistre la température au bout de chaque minute. (Voir résultats ci-dessous)
a) Eau salée :
| Temps (min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 9 | 12 | 15 | 20 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Température (°C) | 41 | 52 | 64 | 75 | 88 | 100 | 103 | 104 | 105 | 105 | 106 |
| État physique | Liquide | Liquide + gaz | |||||||||
b) Eau distillée (eau pur) :
| Temps (min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 10 | 11 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Température (°C) | 30 | 42 | 53 | 65 | 77 | 88 | 100 | 100 | 100 | 100 | 100 |
| État physique | Liquide | Liquide + gaz | |||||||||
c) Glace d’eau distillế :
| Temps (min) | 0 | 1 | 2 | 3 | 5 | 6 | 8 | 10 | 11 |
|---|---|---|---|---|---|---|---|---|---|
| Température (°C) | -6 | -4 | -2 | -1 | 0 | 0 | 4 | 5 | 7 |
| État physique | Solide | Solide + liquide | Liquide | ||||||
2) Observation:
* L’évaporation de l’eau salée ne se fait pas à température constante.
* Lors de l’évaporation de l’eau distillée, la température reste constante. On observe un palier de température à $100^{\circ} \mathrm{C}$.
* Lorsqu’on chauffe la glace d’eau distillée, sa température augmente puis elle reste constante à $0^{\circ} \mathrm{C}$ pendant toute la fusion, puis augmente à nouveau.
3) Conclusion :
* L’évaporation de l’eau pure s’effectue à température constante et égale à $100^{\circ} \mathrm{C}$.
* La fusion de la glace de l’eau pure s’effectue à température constante et égale à $0^{\circ} \mathrm{C}$.
* Un corps pur est caractérisé par une température d’évaporation et une température de fusion constantes.
II. Quelques exemples de corps purs :
Exercice 1:
$1)$ Donner la définition de corps pur.
$2)$ Donner les caractéristiques.
$3)$ Placer les mots suivants dans la bonne place : Solide – substance – température -Liquide – gaz – corps pur
– Un corps est appelé $………………..$ lorsqu’il ne contient qu’une seule $………………..$
– Un corps pur peut un être $……………..$, un $………………..$ ou un $………………$
– Pour un corps pur la $………………..$ ne change pas pendant le changement d’état
$1)$ Un corps pur est une substance qui ne contient qu’un seul type de constituant (molécule ou atome).
Il n’est pas un mélange et possède une composition chimique constante.
$2)$
• Il a une composition uniforme.
• Il possède une température de fusion et d’ébullition constante (ex. : l’eau pure bout à $100 °C$, fond à $0 °C$ à pression normale).
• Il ne peut pas être séparé en plusieurs constituants par des méthodes physiques simples (filtration, décantation…).
• Il peut être solide, liquide ou gaz à l’état pur.
$3)$
– Un corps est appelé corps pur lorsqu’il ne contient qu’une seule substance
– Un corps pur peut un être solide , un liquide ou un gaz.
– Pour un corps pur la température ne change pas pendant le changement d’état
Exercice 2:
Entourer la bonne réponse:
$1)$ La température d’ébullition (vaporisation) de l’eau sucrée est:
$100 °C$ – inférieur à $100 °C$ – supérieur à $100 °C$
$2)$ Lors de la solidification d’un corps pur, sa température :
Augmente – ne change pas – diminue
$3)$ La masse volumique de l’eau salée peut prendre :
Seule valeur – deux valeurs – plusieurs valeurs
$4)$ Le café au lait préparé au petit déjeuné est un :
Mélange hétérogène – corps pur – mélange homogène
Exercice 3:
Réponds par Vrai ou par Faux
– Tous les corps purs sont homogènes $…………$
– Une substance qui n’est pas un mélange est un corps pur $…………$
– Toutes les substances homogènes sont des corps purs $…………$
– Une eau claire est un corps pur $…………$
Exercice 4:
On fait chauffer deux liquides $A$ et $B$ séparés ; lors de l’ébullition on repère la température de chaque liquide au bout d’une minute. on obtient les résultats suivants :
| Durée en min | 0 | 1 | 2 | 3 | 4 | 5 |
|---|---|---|---|---|---|---|
| Température du liquide A en °C | 76 | 77 | 78 | 78 | 78 | 78 |
| Température du liquide B en °C | 74 | 76 | 78 | 80 | 81 | 82 |
$1)$ Quel est le liquide qui représente un corps pur
$2)$ Quel est le liquide qui représente un mélange
Exercice 5:
On mesure la masse et le volume du café noire et de l’eau distillée, on obtient les résultats suivants .
| Solution | Eau distillée | Eau distillée | Eau distillée | Café au lait | Café au lait | Café au lait |
|---|---|---|---|---|---|---|
| m : la masse (g) | 23 | 112 | 489 | 70 | 117 | 415 |
| V : le volume (cm³) | 23 | 112 | 489 | 50 | 78 | 256 |
| ρ : masse volumique (g/cm³) |
$1)$ Calculer la masse volumique et remplir le tableau au-dessus.
$2)$ Quelle est la solution qui représente un corps pur, justifier votre réponse .
$3)$ Quelle est la solution qui représente un mélange, justifier votre réponse .
Exercice 6:
Choisir les noms de ces légendes parmi : corps pur ; mélange homogène ; mélange hétérogène
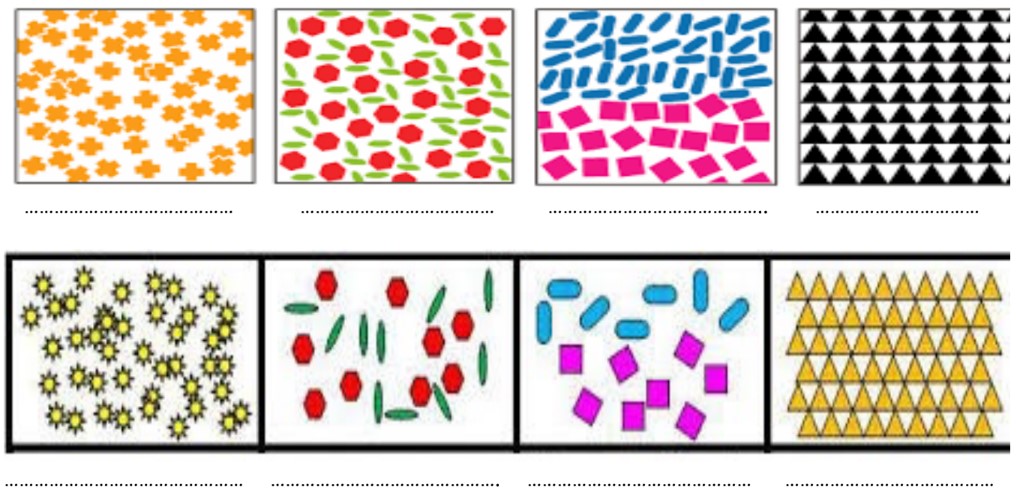
Exercice 7:
Voici les températures de fusion et de l’ébullition de quelques corps purs.
Donner leur état à $- 45 °C, 2 °C, 80 °C $.
| Fusion | Ébullition | État à -45°C | État à 2°C | État à 80°C | |
|---|---|---|---|---|---|
| Alcool | -117°C | 69°C | – | – | – |
| Fer | 1538°C | 2861°C | – | – | – |
Exercice 8:
Partie 1 : Questions de cours
$1)$ Qu’est-ce qu’un corps pur ? Donnez deux exemples.
$2)$ Citez deux caractéristiques importantes d’un corps pur lors des changements d’état.
$3)$ Quelle est la température de fusion de l’eau pure ? Et sa température d’ébullition ?
Partie 2 : Analyse de données
On a relevé les températures de changement d’état de trois substances :
| Substance | Fusion (°C) | Ébullition (°C) |
|---|---|---|
| A | 0 | 100 |
| B | -117 | 78 |
| C | 1538 | 2862 |
$4)$ Identifiez chaque substance $(A, B, C)$ en justifiant votre réponse.
$5)$ Dans quel état se trouve la substance $B$ à $25°C$ ? Et à $-120°C$ ?
Partie 3 : Expérience
$6)$ On chauffe un mélange d’eau salée et de l’eau pure séparément. Observe-t-on la même température pendant toute la durée de l’ébullition ? Expliquez.
La chaleur et les changements d’état physique de la matière exercices corrigés
