Le modèle de l’atome – Cours
Le modèle de l’atome
I-L’évolution historique de l’atome :
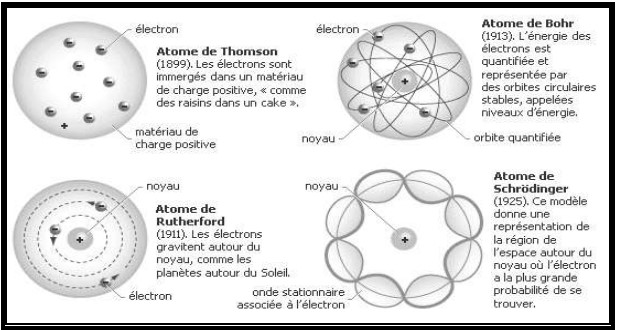
II-Structure de l’atome :
1-Modélisation de l’atome :
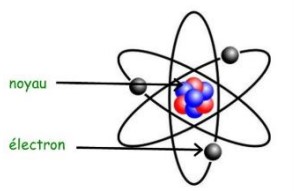
Le modèle de l’atome est constitué d’un noyau autour duquel gravitent des électrons.
Les électrons tournent autour du noyau dans une zone sphérique délimitant la taille de l’atome appelée nuage électronique.
Le noyau de l’atome est constitué de particules appelés nucléons, les neutrons et les protons.
2-Constituants de l’atome :
L’atome est constitué d’un noyau et d’électrons.
2-1-Les électrons :
La masse de l’électron e– est : me = 9,11.10-31 kg
Sa charge électrique est : qe = -e = -1,6.10-19 C
Remarque : e est appelé charge élémentaire e = 1,6.10-19 C
2-2-Le noyau :
Il est constitué de particules élémentaires : les protons et les neutrons appelés nucléons.
| Proton p | Neutron n |
|---|---|
| Chargé positivement : e = 1,6.10-19 C sa masse : mp = 1,673 .10-27 kg | Particule neutre électriquement sa masse : mn = 1,675 .10-27 kg |
Le nombre de protons du noyau s’appelle le nombre de charge ou le numéro atomique et se note Z.
Le nombre total des nucléons (protons et neutrons) est noté : A = Z + N
N est le nombre total de neutrons.
Remarques :
- La masse du proton et la masse du neutron sont identiques
- La masse du proton est 1836 fois la masse de l’électron mp = 1836 me
- Un atome est électriquement neutre, il possède autant de protons que d’électrons.
3-Symbole du noyau atomique :
On représente le noyau d’un atome par le symbole :

A: nombre de masse
Z: numéro atomique
X: symbole de l’élément chimique
| L’atome | symbole | numéro atomique Z | nombre de nucléons A | nombre de neutrons N |
|---|---|---|---|---|
| Hydrogène | 1H1 | 1 | 1 | 0 |
| Oxygène | 16O8 | 8 | 16 | 8 |
| Chlore | 35Cl17 | 17 | 35 | 18 |
4-Masse de l’atome :
La masse de l’atome = la masse du noyau + La masse des électrons
matome = mnoyau + mélectrons
matome = Z.mp + (A – Z).mn + Z.mélectrons
La masse des électrons est négligeable devant celle des nucléons (mp ≈ mn ≈ 1836 me) :
matome = Z.mp + (A – Z).mn
III- L’élément chimique :
1-Isotope :
Les isotopes sont des atomes qui ont mêmes numéro atomique Z et des nombres de nucléons A différents (ils différent par leur nombre de neutrons).
Exemple isotopes de carbone Z=6:
12C 13C 14C
Exemples : Na+ ; Al3+
Un atome qui gagne des électrons devient chargé négativement est un anion.
Exemples : Cl– ; O2-
IV-Répartition des électrons d’un atome :
1-Les couches électroniques :
Les électrons sont en mouvement autour du noyau : on parle du « cortège électronique » du noyau.
Les électrons d’un atome se répartissent dans des couches électroniques autour du noyau. Chaque couche est représentée par une lettre K, L, M pour les atomes qui ont Z ≤ 18.
2-Règles de remplissage des couches électroniques :
Première règle : Une couche électronique ne peut contenir qu’un nombre limité d’électrons.
- La couche K (première couche) peut contenir un maximum de 2 électrons.
- La couche L (deuxième couche) peut contenir un maximum de 8 électrons.
- La couche M (troisième couche) peut contenir un maximum de 8 électrons.
Deuxième règle : Le remplissage des couches électroniques s’effectue en commençant par la couche K. Lorsqu’une couche est saturée on remplit la couche L et ainsi de suite.
Remarque : Lorsqu’une couche est pleine on dit qu’elle est saturée.
3-Structure électronique de l’atome :
La structure électronique est composée des lettres correspondant aux couches K, L, M écrites entre parenthèses. On place en exposant en haut à droite, le nombre d’électrons présents dans la couche.
La dernière couche de la structure électronique est appelée couche externe. Les autres occupés par les électrons sont nommées couches internes.
Exemples :
- L’atome de soufre S : Z = 16. La structure électronique : (K)²(L)⁸(M)⁶
- L’ion aluminium Al³⁺ : Z = 13
L’atome d’aluminium possède 13 électrons, il a perdu 3 électrons, il reste 10 électrons. La structure électronique : (K)²(L)⁸
Le modèle de l’atome – Cours
