le cours sur les atomes et les ions en classe de 3ème revêt un intérêt considérable, car elle constitue la base de la compréhension de la chimie et de la matière.
Comprendre la structure de base de la matière au niveau atomique permet aux élèves de saisir comment les éléments chimiques réagissent entre eux pour former des composés, et comment les réactions chimiques se produisent. les atomes et les ions

1- Les Constituants de l’atome :
L’atome est constitué d’un noyau entouré d’électrons formant un nuage électronique.
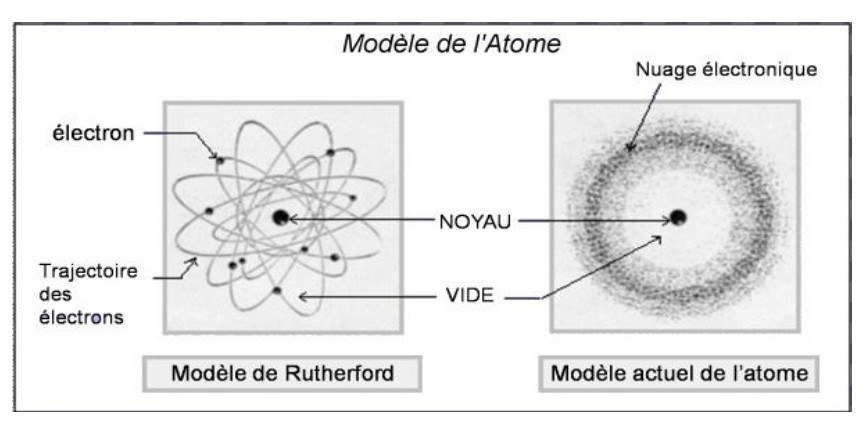
2- Le noyau :
- Le noyau est situé au centre de l’atome.
- Noyau porte des charges électriques positives.
- Le diamètre du noyau est plus petit que le diamètre de l’atome.
- Diamètre du noyau est 100 000 fois plus petit que le diamètre de l’atome.
- La masse d’un atome est pratiquement égale à la masse de son noyau. les atomes et les ions
3- Les électrons :
- Les électrons forment le nuage électronique.
- tous les électrons sont identiques même s’ils appartiennent à des atomes différents.
- Les électrons ont une masse très faible (négligeable).
- Tous les électrons portent des charges électriques négatives.
- Chaque électron porte une charge électrique négative notée ( – e )
- «e» représente la charge élémentaire, exprimée en coulomb sa valeur est e = 1,6 x10-19
- « C » symbole du coulomb qui est l’unité de mesure légale de la charge électrique .
4- L’électroneutralité de l’atome:
Un atome est électriquement neutre, car le nombre de charges électriques positives de son noyau est égal au nombre de charges électriques négatives de ses électrons.
5- numéro atomique :
le numéro atomique est le nombre de charges positives contenu dans le noyau, il est noté Z .
Exercice N°1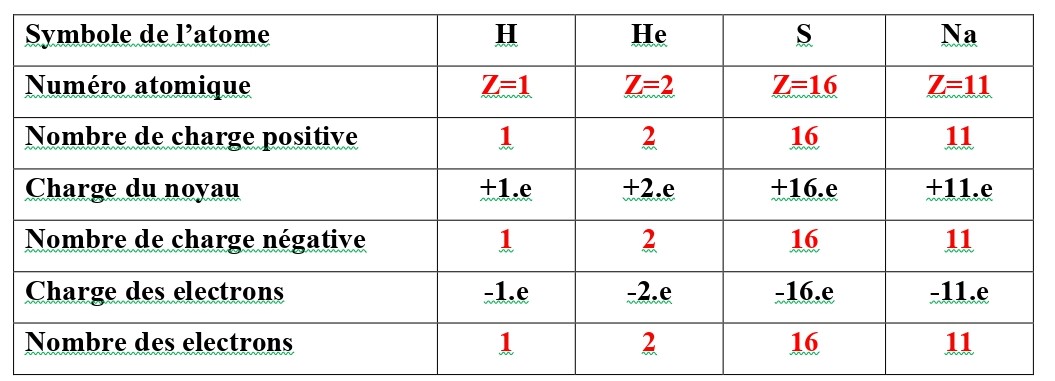
Remarque :
Dans un atome de charge électrique neutre, le numéro atomique Z représente à la fois le nombre de charge positive du noyau et le nombre de charge négative des électrons et le nombre d’électrons.
Exercice N°2

Conclusion :
- chaque atome est caractérisé par son numéro atomique noté Z.
- La charge totale du noyau d’ un atome exprimer en fonction de la charge élémentaire par +Z.e
- La charge totale des électrons d’un atome exprimer en fonction de la charge élémentaire par ─ Z.e
- Charge d’un atome est nulle on dit que l’ atome est électriquement neutre
( + Z.e ) + ( ─ Z.e ) = 0.e = 0 les atomes et les ions
Voir aussi
