Les atomes et les ions exercices corrigés
Matériaux et électricité
I. L’atome : un modèle pour comprendre (structure de l’atome)
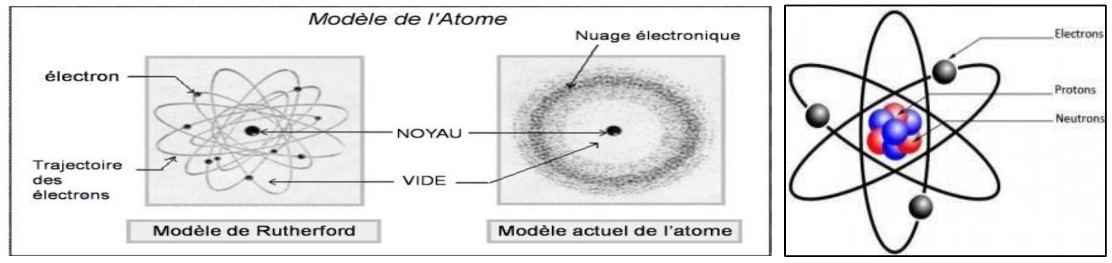
1. Modèles d’atome
– Modèle de BOHR c’est le modèle planétaire les électrons gravitent sur des trajectoires précises.
– Le modèle actuel modélise l’atome par: le noyau qui est entouré d’un nuage électronique (pas de trajectoire) ; c’est le modèle de Scrodinger, modèle probabiliste
– L’atome est constitué d’un noyau entouré d’électrons formant un nuage électronique.
a. Le noyau :
– Le noyau est situé au centre de l’atome et porte des charges positives.
– Toute la masse de l’atome est pratiquement concentrée dans le noyau.
– Le diamètre du noyau est $100000$ fois plus petit que celui de l’atome : l’atome est formé essentiellement du vide : L’atome a une structure lacunaire.
– Le nombre de charges positives du noyau d’un atome est appelé numéro atomique noté $Z $, c’est une caractéristique de l’atome.
b. Les électrons :
– Les électrons tournent autour du noyau à très grande vitesse sur des trajectoires variables, plus ou moins éloignées du noyau. Ils forment un cortège électronique dans un atome.
– La masse des électrons est très faible : $\mathrm{m_{e}}=9,1 \cdot \mathrm{10}^{-31} \mathrm{~kg}$
– Chaque électron porte une charge électrique négative notée – e, qui représente la charge élémentaire, exprimée en coulomb de symbole C , sa valeur est $e=1,6 \times \mathrm{10}^{-19} \mathrm{C}$.
– On symbolise l’électron par ${e}^{-}$
– Les électrons sont identiques quel que soit l’atome.
– Chaque atome a un nombre défini d’électrons.
2. Symbole et nombre d’électrons de quelques atomes:
| Atome | Symbole | Nombre d’électrons |
|---|---|---|
| hydrogène | H | 1 |
| carbone | C | 6 |
| oxygène | O | 8 |
| cuivre | Cu | 29 |
| fer | Fe | 26 |
3. Neutralité électronique de l’atome :
– Dans un atome le nombre de charges positives de son noyau est égal au nombre de charges négatives de ses électrons.
– Ainsi, la charge positive du noyau $( + Ze )$ est opposée à la charge négative du nuage électronique $( -Ze)$.
– La charge totale d’un atome est nulle $( +Ze )$ $+(-\mathrm{Ze})=0$ : l’atome est électriquement neutre.
$ \text { Charge de l’atome }=\text { charge du noyau }+ \text { charge du nuage électronique } $
$ 0=(+\mathrm{Ze})+(-\mathrm{Ze})$
Application :
| Atome | Symbole | Numéro atomique Z | Charge de noyau de l’atome (+Ze) | Charge des électrons de l’atome (-Ze) | Charge d’atome |
|---|---|---|---|---|---|
| Hydrogène | H | 1 | +1 e | -1 e | 0 e |
| Carbone | C | 6 | +6 e | -6 e | 0 e |
| Fer | Fe | 26 | +26 e | -26 e | 0 e |
| Chlore | Cl | 17 | +17 e | -17 e | 0 e |
II. Les ions

1. Définition:
– Un ion est un atome qui a perdu ou gagné un ou plusieurs électrons.
– Certains ions sont constitués d’un seul type d’atome. On les appelle des ions monoatomiques.
– D’autres sont formés par l’association d’atomes de types différents : ce sont des ions polyatomiques.
– Un atome ne peut perdre que des charges négatives.
– Le nombre de protons (charges positives) ne change pas.
– Un anion est un ion négatif. Il a gagné un ou plusieurs électrons.
– Un cation est un ion positif. Il a perdu un ou plusieurs électrons.
2. Les types d’un ion :
On distingue deux types d’ions :
• Les ions positifs appelés cations exemples: $\mathrm{H}^{+}, \mathrm{Cu}^{2+}, \mathrm{NH}^{4+}$
• Les ions négatifs appelés anions exemples: $\mathrm{OH}^{-}, \mathrm{S}^{2-}, \mathrm{HCOO}^{-}$
* Un anion est un atome ou un groupe d’atomes qui a gagné un ou plusieurs électrons.
* Un cation est un atome ou un groupe d’atomes qui perdu un ou plusieurs électrons.
Remarque :
\$ Un ion monoatomique est constitué d’un seul atome.
\$ Un ion poly atomique est constitué par un ensemble d’atomes.
| Les cations | Les anions | ||
|---|---|---|---|
| monoatomiques | polyatomiques | monoatomiques | polyatomiques |
H⁺ Al³⁺ | NH₄⁺ H₃O⁺ | Cl⁻ O²⁻ | OH⁻ SO₄²⁻ |
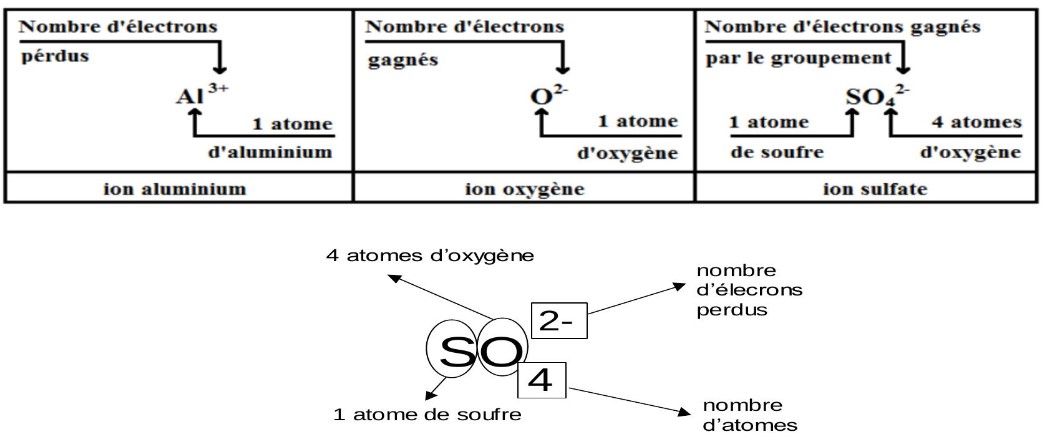
3. formule des ions :
• On représente un ion monoatomique par le même symbole de l’atome en ajoutant en haut et à droite du symbole le nombre de charges et de leur signe ( + ou – ).
• La formule de l’ion poly atomique s’obtient en :
– écrivant la formule de la molécule qui serait formée par ces atomes
– indiquant en exposant le nombre de charges et le signe
• La formule d’un ion monoatomique s’écrit à partir du symbole de l’atome auquel on ajoute en haut et à droite le nombre de charges et de leur signe ( + ou – ).
Exercice 1:
Répond par vrai ou faux :
$1)$ Un cation est un atome ou un groupe d’atomes qui a gagné un ou plusieurs électrons.
$2)$ Un anion est un atome ou un groupe d’atomes qui perdu un ou plusieurs électrons.
$3)$ Un ion monoatomique est constitué d’un seul atome.
$4)$ Un ion poly atomique est constitué par un ensemble d’atomes.
$1)$ Faux
$2)$ Faux
$3)$ Vrai
$4)$ Vrai
Exercice 2:
Compléter les phrases par les mots : -e – noyau – $(-Ze)$ – nuage –positive – négative – $(+Ze)$ – nulle – numéro atomique – gagné – perdu
$1)$ L’atome est constitué d’un $………………..$entouré d’électrons formant un$………………….$électronique
$2)$ La charge de noyau d’un atome est $………………………….$et s’exprime en fonction de $e$ :$ …………………..$
$3)$ Chaque électron porte une charge $……………………….$noté$ ………..$
$4)$ La charge négative des électrons d’un atome s’exprime en fonction de $e$ : $…………….$
$5)$ La charge totale d’un atome est $…………$
$6)$ Le nombre de charges positives du noyau d’un atome est appelé $……………………..$numéro atomique noté $ Z$
$7)$ Un ion est un atome qui a $……………….$ou $…………$un ou plusieurs électrons
Exercice 3:
Classer les ions suivants dans le tableau si dessous : NH4+ , Ca2+ , Cl– ,OH– , Na+ , Mg2+
| Les cations | Les anions | ||
|---|---|---|---|
| monoatomiques | polyatomiques | monoatomiques | polyatomiques |
Exercice 4:
Le noyau de l’atome de silicium $(Si)$ contient $14$ charges positives.
$1)$ Quel est le numéro atomique de l’atome de silicium ?
$2)$ Combien y a-t-il d’électrons dans l’atome de silicium ?
Exercice 5:
Je complète le tableau suivant:
| Atome | Symbole | Numéro atomique Z | Charge d’électron qe | Charge du noyau qn | Charge de l’atome qa |
|---|---|---|---|---|---|
| O | -8 e | ||||
| Al | 13 | ||||
| Na | +11 e | ||||
| Chlore | +17 e | ||||
| Cuivre | 29 |
Exercice 6:
$1)$ l’atome de zinc $(Zn)$ peut passer à l’état d’ion en perdant $2$ électrons. Quelle est la formule de l’ion correspondant ?
$2)$ l’atome de soufre $(S)$ peut passer à l’état d’ion en gagnant $2$ électrons. Quelle est la formule de l’ion correspondant ?
Exercice 7:
L’atome du Zinc $(Zn)$ de numéro atomique $Z=30$ perd $2$ électrons pour devenir un ion.
$1)$ Combien d’électrons dans l’atome du zinc ?
$2)$ Déterminer la charge des électrons de cet atome en coulomb $(C)$.
$3)$ Déterminer la charge du noyau de cet atome en coulomb $(C)$.
$4)$ Déterminer la charge des électrons de l’ion du zinc en coulomb $(C)$.
$5)$ Déterminer la charge du noyau de l’ion du zinc en coulomb $(C)$.
$6)$ Calculer la charge d’ion du zinc en fonction de ‘e’ puis en coulomb $(C)$.
$7)$ Écrire la formule de l’ion.
$8)$ Donner le type de cetion.
Exercice 8:
L’atome du cuivre (Cu) se transforme en ion Cu ${ }^{2+}$. (Z=29)
$1)$ Expliquer cette transformation.
$2)$ Donner la charge des électrons de l’ion $\mathbf{C u}^{\mathbf{2 +}}$ en fonction de la charge élémentaire $e$.
$3)$ Donner la charge du noyau de l’ion $\mathbf{C u}^{2+}$ en fonction de la charge élémentaire $e$.
$4)$ Calculer la charge de cet ion en coulomb $(C)$.
Exercice 9:
Considérons les ions suivants : $\mathrm{Cr}^{3+} ; \mathrm{CH}_{3} \mathrm{COO}^{-} ; \mathrm{SO}_{4}^{2-} ; \mathrm{H}_{3} \mathrm{O}^{+} ; \mathrm{Br}^{-} ; \mathrm{Mg}^{2+} ; \mathrm{NO}_{3}^{-}$.
$1)$ Classer ces ions suivants. (Anions/cations et ions monoatomiques/ions polyatomiques)
$2)$ La charge totale des électrons de l’ion $\boldsymbol{C r}^{\mathbf{3 +}}$ est : $\boldsymbol{q}_{\boldsymbol{e}}=-33.6 \times \mathbf{1 0}^{-\mathbf{1 9}} \mathrm{C}$.
$a)$ Trouver le numéro atomique de l’atome du chrome.
$b)$ Calculer en coulomb C la charge du noyau $\boldsymbol{q}_{\boldsymbol{n}}$ de cet atome.
$c)$ Calculer en coulomb C la charge des électrons $q_{e}$ de cet atome.
$d)$ Déduire $\boldsymbol{q}_{\boldsymbol{a}}$ la charge de l’atome.
Exercice 10:
$1)$ Le noyau de l’atome de calcium $(Ca)$ contient $20$ charges positives. On donne :
$a)$ Donner le numéro atomique $Z$ de l’atome de calcium.
$b)$ Déterminer en fonction de $(e)$ et en coulomb, $Q_{n}$ la charge de noyau de cet atome.
$c)$ Déterminer en fonction de $(e)$ et en coulomb, $Q_{e}$ la charge des électrons de cet atome.
$d)$ Calculer $Q_{a}$ la charge globale de l’atome.
$2)$ L’atome de calcium peut perdre deux électrons pour donner l’ion calcium.
$a)$ Ecrire la formule chimique de l’ion calcium et donner son type.
$b)$ Déterminer le nombre des électrons de l’ion calcium.
$c)$ Déterminer en fonction de $(e)$, $Q_{e}$ la charge des électrons de l’ion calcium.
$d)$ Calculer en fonction de $(e)$ la charge de l’ion calcium.
Exercice 11:
L’atome de fer $(\mathrm{Fe})$ se transforme en ion $\mathrm{Fe}^{2+}$.
On donne $\mathrm{Z}(\mathrm{Fe})=26$ et $\mathrm{e}=1,6 \cdot {10}^{-19} \mathrm{C}$.
$1)$ Expliquer cette transformation
$2)$ Donner la charge des électrons d’ion $\mathrm{Fe}^{2+}$ en fonction de $e $
$3)$ Donner la charge du noyau d’ion $\mathrm{Fe}^{2+}$ en fonction de $e$
$4)$ Calculer la charge d’ion $\mathrm{Fe}^{2+}$ en coulomb $C$
Exercice 12:
Le symbole d’un ion set: $\mathrm{NH}_{4}^{+}$
$1)$ Donner le type de ion
$2)$ Quelle est la charge d’ion $\mathrm{NH}_{4}^{+}$ en fonction de $e$
$3)$ Calculer la charge d’ion $\mathrm{NH}_{4}^{+}$ en coulomb $C$
$4)$ Calculer le nombre d’électrons d’ion
On donne : $Z(N)=7$ et $Z(H)=1$
Exercice 13:
Complétez le tableau suivant :
| Atome | Ion | |||||||
|---|---|---|---|---|---|---|---|---|
| Atome | Numéro Atomique | Charge des électrons | Charge du noyau | Nombre des électrons | Charge des électrons | Charge du noyau | Formule de l’ion | Charge D’ion |
| Cu | +29e | 27 | ||||||
| S | 16 | -2e | ||||||
| Al | +13e | Al³⁺ | ||||||
| F | -7e | 8 | ||||||
Les atomes et les ions exercices corrigés
