Réactions chimiques exercices corrigés 2AC
Notion de réaction chimique
I. Notion de réaction chimique
1. La combustion de l’alcool dans l’air
A. Expérience
On réalise la combustion de l’alcool dans l’air. L’entonnoir est placé au-dessus de la flamme bleue.
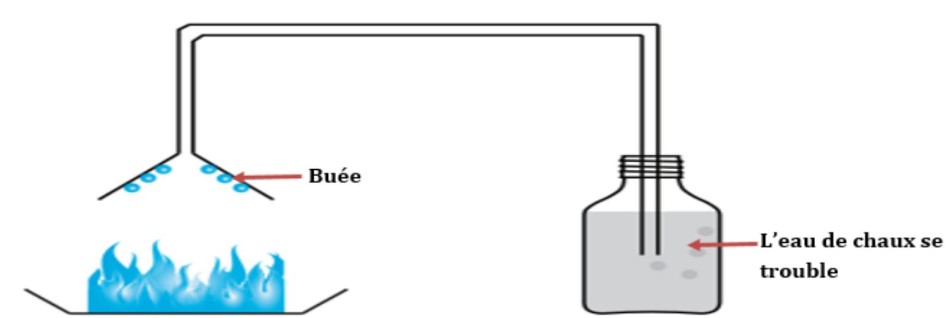
B. Observation
On constate de la buée sur les parois de l’entonnoir.
On constate que l’eau de chaux se trouble dans le flacon.
Après un certain temps, il disparait de l’alcool et la combustion s’arrête.
C. Conclusion
La combustion de l’alcool dans l’air est une transfomration chimique au cours de laquelle, il disparait l’alcool et le dioxygène et il apparait deux nouveaux corps : l’eau et le dioxyde de carbone. Cette transformation chimique s’appelle une réaction chimique.
La combustion de l’alcool dans l’air s’arrête lorsque l’alcool se consomme.
On peut exprimer le bilan de cette réaction chimique par l’écriture suivante:
$\text { Alcool }+ \text { Dioxygène } \rightarrow \text { eau + dioxyde de carbone }$
2. Définition de la réaction chimique
La réaction chimique est une transformation au cours de laquelle, des corps disparaissent appelés réactifs et des corps apparaissent appelés réactifs.
3. Quelques exemples des réactions chimiques
Exemple 1: Réaction entre le fer et le soufre
$\text { Fer }+ \text { Soufre } \rightarrow \text { Sulfure de fer }$
Exemple 2: Combustion du fer dans le dioxygène
$\text { Fer }+ \text { Dioxygène } \rightarrow \text { Oxyde de fer }$
Exemple 3: Combustion complète du méthane dans le dioxygène
$\text { Méthane + Dioxygène } \rightarrow \text { Eau + Dioxyde de carbone }$
Exemple 4: Combustion du soufre dans le dioxygène
$\text { Soufre }+ \text { Dioxygène } \rightarrow \text { Dioxyde de soufre }$
Exemple 5: Synthèse de l’eau (réaction entre le dihydrogène et le dioxygène)
$\text { Dihydrogène }+ \text { Dioxygène } \rightarrow \text { Eau }$
II.Transformation physique et transformation chimique
A.Expérience
On place dans un récipient, des tronçons de glace d’eau sortis d’un congélateur.
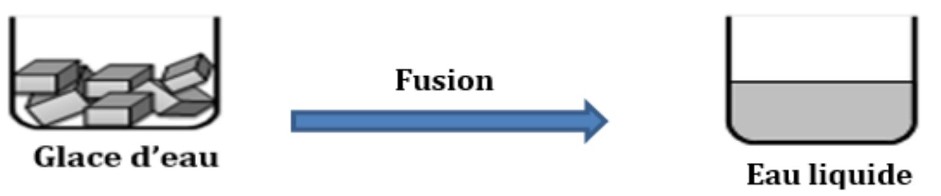
B.Observation
Durant la fusion de la glace,L’eau passe de l’état physique solide à l’état physique liquide :Cette transformation s’appelle une transformation physique.
La fusion est le passage de l’état physique solide à l’état physique liquide.
C.Conclusion
Lors d’une transformation chimique,des corps se consomment appelés réactifs pour donner d’autres corps appelés produits.
Lors d’une transformation physique,un corps change d’état physique.Les particules constituant ce corps ne sont pas modifiées.
Remarque:
Lorsqu’un corps passe d’un état physique à un autre,on dit qu’il y a changement d’état :
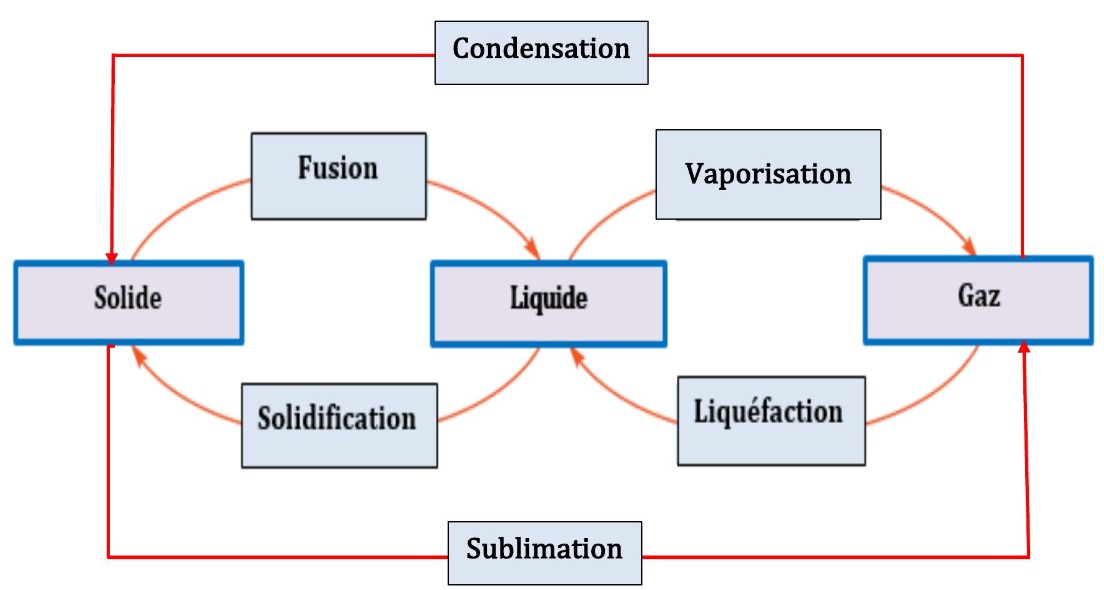
• la vaporisation :est le passage de l’état liquide à l’état gazeux,lorsqu’un corps se vaporise,il reçoit de la chaleur et passe à l’état gazeux.Ce passage peut porter d’autres noms comme l’évaporation ou la vaporisation par ébullition.
• L’évaporation qui se produit lentement en surface du liquide à toute température.
• La vaporisation par ébullition qui se produit rapidement à température constante.
Exercice 1:
Complète les phrases suivantes avec les mots : réactifs, produits, réaction chimique, transformation physique.
• Lors d’une $………………..$, les corps initiaux disparaissent pour former de nouveaux corps.
• Les substances qui réagissent au début sont appelées $………………..$.
• Les substances obtenues à la fin sont appelées $………………..$ .
• La fusion de la glace est un exemple de $………………..$ .
• Lors d’une réaction chimique , les corps initiaux disparaissent pour former de nouveaux corps.
• Les substances qui réagissent au début sont appelées réactifs.
• Les substances obtenues à la fin sont appelées produits .
• La fusion de la glace est un exemple de transformation physique .
Exercice 2:
Lors de la combustion de l’alcool dans l’air :
– On observe de la buee sur les parois de l’entonnoir.
– L’eau de chaux se trouble.
– L’alcool finit par disparaître.
$1)$ Quelle transformation a lieu? Justifie.
$2)$ Quels sont les reactifs?
$3)$ Quels sont les produits?
$4)$ Écris le bilan de la reaction.
Exercice 3:
Indique si les transformations suivantes sont physiques ou chimiques:
• Glace qui fond : $…………$
• Fer + soufre -> sulfure de fer : $…………$
• Eau qui bout : $…………$
• Dihydrogène + dioxygène -> eau : $…………$
Exercice 4:
Donne l’equation des reactions chimiques suivantes avec les noms des reactifs et des produits:
$1)$ Réaction entre le fer et le soufre
$2)$ Combustion du fer dans le dioxygène
$3)$ Combustion complète du méthane dans le dioxygène
$4)$ Combustion du soufre dans le dioxygène
$5)$ Synthèse de l’eau (réaction entre le dihydrogène et le dioxygène)
Exercice 5:
Répondre par Vrai ou Faux :
$1)$ Les produits sont identiques aux reactifs. : $……….$
$2)$ La vaporisation est une transformation physique. : $……….$
$3)$ La combustion est une transformation chimique. : $……….$
$4)$ Les particules du corps sont modifiées. : $……….$
Exercice 6:
Voici une description d’une transformation. Repere et corrige les erreurs :
« Lors de la combustion du fer dans l’air, le fer se transforme en dioxygene et en eau.«
Exercice 7:
Écris le nom des réactifs et des produits pour les équations suivantes :
$1)$ $\mathrm{CH_{4}} +2\mathrm{O_{2}} \rightarrow \mathrm{CO_{2}} +2\mathrm{H_{2}O} $
$b)$ $4\mathrm{Fe}+3\mathrm{O_{2}}\rightarrow 2\mathrm{Fe_{2}} \mathrm{O_{3}} $
Exercice 8:
Un élève affirme : « La vaporisation est une reaction chimique car on ne voit plus le liquide. »
Explique pourquoi cette affirmation est fausse.
Exercice 9:
La combustion du methane ne se produit pas si on n’apporte pas d’energie (flamme).
$1)$ Quelle est la condition necessaire pour qu’une reaction chimique ait lieu?
$2)$ Donne un autre exemple où une condition est necessaire.
Exercice 10:
La combustion de l’argent dans le dioxygène conduit à la formation de l’oxyde de l’argent.
$1)$ Indiquer les réactifs dans cette réaction chimique.
$2)$ Quel est le produit de cette réaction chimique?
$3)$ Écrire le bilan littéral de la réaction ?
Exercice 11:
L’aluminium ($Al$) réagit avec le dioxygène, pour former l’oxyde d’aluminium ($\mathrm{Al}_{2} \mathrm{O}_{3}$) .
$1)$ Donnez le bilan littéral de cette réaction .
$2)$ Donnez l’équation bilan de cette réaction .
Réactions chimiques exercices corrigés 2AC
