Synthèse des espèces chimiques – exercices corrigés
Exercice 1: Questions de cours
Réponses correctes :
- Il peut se former plusieurs produits;
dont certains peuvent être des sous-produits ou des impuretés.
Réponses correctes :
- On peut ajouter un catalyseur;
- On peut chauffer le mélange réactionnel;
pour accélérer une réaction chimique. La condensation des vapeurs est une technique de reflux,
pas une méthode d’accélération.
Réponse correcte :
- L’eau circule de bas en haut;
un remplissage complet du réfrigérant et une efficacité maximale du refroidissement.
Réponses correctes :
- La transformation est accélérée;
- Les vapeurs formées se condensent;
la perte de réactifs ou de solvant grâce à la condensation des vapeurs. Un catalyseur n’est pas
nécessaire pour utiliser cette technique.
Réponse correcte :
- De vérifier la présence et la pureté de l’espace synthétisé;
et la pureté d’un produit, mais pas de le purifier ou de l’isoler du mélange réactionnel.
Réponses correctes :
- Peut-être mélangée à d’autres espèces;
- Est extraite du mélange réactionnel.
(solvant, catalyseur, sous-produits). Il faut généralement procéder à une extraction et une purification
pour isoler le produit souhaité.
Exercice 2: Synthèse de l’acétate de menthyle
L’acétate de menthyle est un ester qui amplifie la touche « florale » des eaux de lavande commerciales.
On le prépare à partir d’acide acétique et de menthol. Pour synthétiser cet ester, on introduit dans un ballon à fond rond de l’acide acétique, du menthol, quelques gouttes d’acide sulfurique concentré (très soluble dans l’eau) et de la pierre ponce. On adapte un réfrigérant à eau vertical sur le ballon. On chauffe à reflux pendant 1H30min.
| Espèce chimique | Menthol | Acide acétique | Acétate de menthyle |
|---|---|---|---|
| Température de fusion (°C) | 41 | 16 | 0 |
| Température d’ébullition (°C) | 212 | 118 | 227 |
| Densité | 0,89 | 1,05 | 0,92 |
| Solubilité dans l’eau | Faible | Grande | Très faible |
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 3: L’arôme de Jasmin
La chimie de synthèse s’avère indispensable pour pallier les insuffisances des productions naturelles ou les coûts élevés de production de certaines espèces chimiques naturelles. 120 000 pétales de rose sont nécessaires à la production de 15 mL d’huile essentielle pure de rose. Pour obtenir seulement 1 kg d’huile essentielle pure de jasmin il faut environ 8 millions de bourgeons de jasmin récoltés à la main. Les chimistes ont donc cherché à synthétiser ces espèces présentes dans la nature. On se propose d’étudier la synthèse de l’acétate de benzyle, molécule à l’odeur de jasmin.
Partie A : La synthèse
Protocole expérimental :
Placer dans un ballon 12,0 cm³ d’alcool benzylique, 15,0 cm³ d’acide acétique, quelques gouttes d’acide sulfurique (pour accélérer la réaction) et quelques grains de pierre ponce. Réaliser un montage de chauffage à reflux. Chauffer pendant 30 minutes.
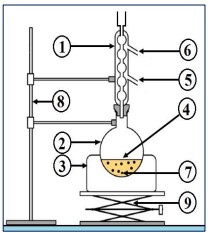
| Espèce chimique | Alcool benzylique | Acide acétique | Acétate de benzyle | Eau salée |
|---|---|---|---|---|
| Masse volumique (g/cm³) | 1,04 | 1,05 | 1,06 | 1,25 |
Partie B : L’extraction
Protocole expérimental :
Après avoir refroidi le mélange réactionnel, verser le contenu du ballon dans une ampoule à décanter, ajouter 50 mL d’une solution aqueuse saturée de chlorure de sodium (densité 1,25). Après avoir agité et laissé décanter, recueillir la phase contenant l’acétate de benzyle. Lors de la synthèse, on admettra que tous les réactifs n’ont pas complètement réagi et qu’il en reste dans le mélange réactionnel.
| Espèce chimique | Alcool benzylique | Acide acétique | Acétate de benzyle | Eau salée |
|---|---|---|---|---|
| Solubilité dans l’eau | faible | Totale | faible | Totale |
| Solubilité dans l’eau salée | faible | totale | Nulle |
Partie C : Caractérisation de l’espèce chimique synthétisée
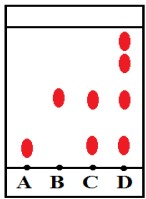
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 4: Synthèse de l’essence de lavande
Pour synthétiser l’éthanoate de linalyle, principal constituant de l’essence de lavande. On suivie le Protocole expérimental suivant:
- Dans un ballon de 250 mL, verser 30 mL de linalol, 90 mL d’acide éthanoïque et 1 mL d’acide sulfurique. Chauffer à reflux pendant une heure.
- Après refroidissement du ballon, verser le contenu dans une ampoule à décanter. Ajouter l’eau salée et agiter vigoureusement. Laisser décanter, puis éliminer la phase aqueuse.
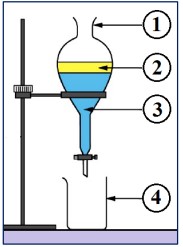
Afin de vérifier l’identité du produit obtenu, on réalise une chromatographie.

- Quelle est l’utilité du chauffage à reflux ?
- Quelle masse d’acide éthanoïque a-t-on utilisée ? Quelle masse de linalol a-t-on utilisée ?
- Le protocole fait intervenir une ampoule à décanter. Quelle est son utilité ? Indiquer sur le schéma ci-contre les positions de l’eau et de l’éthanoate de linalyle et Indiquer ce que représente chaque numéro de la légende du montage.
- Commenter le chromatogramme obtenu ci-joint.
- A-t-on réalisé la synthèse de l’éthanoate de linalyle ? Si oui, le produit synthétisé est-il pur ? Justifier votre réponse.
Données:
– L : linalol pur; AL : éthanoate de linalyle pur; HE : huile essentielle de lavande; ALS : produit de synthèse.
| Espèce chimique | linalol | Acide éthanoïque | Ethanoate de linalyle | Eau |
|---|---|---|---|---|
| Masse volumique (g/mL) | 0,87 | 1,05 | 0,90 | 1,00 |
| Solubilité dans l’eau salée | Nulle | Grande | Nulle |
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 5: Synthèse de paracétamol
Le paracétamol (connu sous le nom commercial de Doliprane ou Efferalgan) est obtenu par action du para-aminophénol solide sur l’anhydride acétique. Pour la synthèse, on doit dissoudre le para-aminphénol dans de l’eau acidifiée. Le protocole est le suivant:
«On introduit dans un erlenmeyer 6g de para-aminophénol, 50 mL d’eau et 4 mL d’acide acétique pur. Le mélange est placé sous agitation dans un bain-marie à 80°C, jusqu’à disparition du solide. Il est ensuite refroidi en plongeant l’erlenmeyer dans un bain d’eau froide. On ajoute délicatement millilitre par millilitre l’anhydride acétique. On refroidit et on observe la cristallisation du paracétamol. On filtre alors sur Büchner et on sèche les cristaux.»
Une mesure du point de fusion des cristaux obtenus indique \( 161^\circ C \). En théorie, le point de fusion des cristaux est de \( 168^\circ C \).
- Que réalise le manipulateur lorsqu’il met sous agitation, le para-aminophénol, l’eau et l’acide acétique?
- Citer les conditions expérimentales requises pour la synthèse.
- A partir de quelle phrase, du protocole, la synthèse proprement dite démarre-t-elle ?
- Quelle est l’avantage de la filtration sur Büchner ?
- Comment interpréter le fait que le point de fusion ne soit pas exactement égal à \( 168^\circ C \) ?
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 6: Aromatisant à goût de banane
L’acétate de 3-méthylbutyle est une espèce chimique qui possède une odeur caractéristique de banane. On le prépare en deux étapes puis on le caractérise par chromatographie.
Synthèse de l’espèce chimique (étape 1)
- Dans un ballon, on introduit du 3-méthylbutan-1-ol (ou alcool isoamylique), de l’acide acétique, quelques gouttes d’acide sulfurique (catalyseur) et quelques grains de pierre ponce.
- On chauffe le contenu du ballon à reflux pendant une demi-heure (30 min).
Extraction de l’espèce chimique (étape 2)
- On refroidit le ballon et on verse son contenu dans un bécher contenant de l’eau froide.
- On introduit ensuite le mélange dans une ampoule à décanter et on écarte la phase aqueuse.
Purification de la phase organique (étape 3)
- La phase organique est recueillie dans un bécher puis lavée avec une solution saturée de chlorure de sodium. De nouveau, la phase aqueuse est écartée par décantation.
- Le liquide surnageant recueilli a une odeur caractéristique de banane.
- Dans cette phase organique, on introduit environ une spatule de sulfate de magnésium anhydre (solide blanc).
Chromatographie sur couche mince (étape 4)
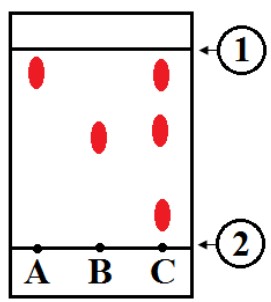
On analyse par chromatographie ce liquide. Pour cela on effectue trois dépôts :
- Dépôt A : solution de 3-méthylbutan-1-ol (ou alcool isoamylique)
- Dépôt B : le liquide obtenu après purification (3)
- Dépôt C : solution d’acétate de 3-méthylbutyle (ou acétate d’isoamyle espèce chimique pure achetée dans le commerce)
- Faire le schéma annoté d’un montage à reflux avec réfrigérant à eau. Sur le schéma annoté d’un montage à reflux avec réfrigérant à eau on trouvera le vocabulaire suivant : élévateur, chauffage, ballon, contenu du ballon, colonne réfrigérante, entrée et sortie d’eau pour le réfrigérant à eau.
- Quel est le rôle du condenseur ? et celle de la pierre ponce ? et celle de l’acide sulfurique ?
- Schématiser l’ampoule à décanter et indiquer les différentes phases et ce qu’elles contiennent. Justifier ta réponse en utilisant pour cela le tableau des données.
- Pourquoi ajoute-t-on du chlorure de sodium ?
- Dans une phase organique on introduit du sulfate de magnésium anhydre (solide blanc). Que signifie le terme « anhydre » ? Quel est le but de cette opération ?
- Décrire rapidement les opérations permettant de réaliser la chromatographie.
- Quel est le rôle joué par l’éluant dans une chromatographie ?
- Voici le résultat de la chromatographie. Compléter le schéma. Identifier A et B et conclure en ce qui concerne l’espèce chimique obtenue après synthèse et extraction.
Données:
| Espèce chimique | Masse Volumique (g/mL) | Température d’ébullition (°C) | Solubilité dans l’eau | Solubilité dans l’eau salée |
|---|---|---|---|---|
| Acide acétique | 1,05 | 118 | Très grande | grande |
| 3-méthylbutan-1-ol (Alcool) | 0,81 | 128 | faible | Nulle |
| Acétate de 3-méthylbutyle (Arôme de banane) | 0,87 | 142 | Très faible | Très faible |
| Acide sulfurique | 1,05 | 330 | Très très grande | Très grande |
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Synthèse des espèces chimiques – exercices corrigés
