Tests de reconnaissance de quelques ions exercices corrigés
Tests de reconnaissance de quelques ions exercices corrigés
I – Test de reconnaissance de l’ion chlorure $\mathbf{C \ell}^{-}$.
1 ) Expérience :
2 ) Observation et interprétation :
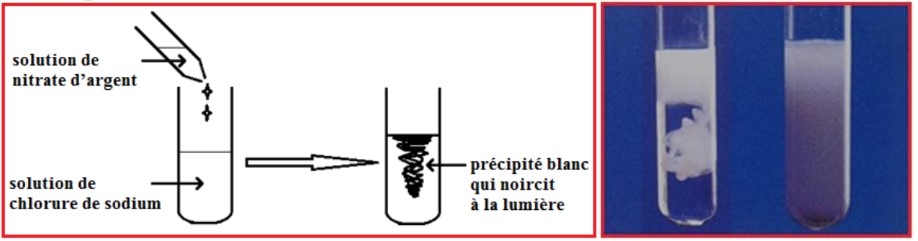
– Lorsque l’on verse quelques gouttes de la solution de nitrate d’argent ( $\mathrm{Ag}^{+}+\mathrm{NO}_{3}{ }^{-}$) dans une solution contenant des ions chlorure $\mathrm{Cl}^{-}$(solution de chlorure de sodium ( $\mathrm{Na}^{+}+\mathrm{Cl}^{-}$) par exemple), il se forme un précipité blanc de chlorure d’argent AgCl qui noircit à la lumière.
– Cette réaction constitue le test de reconnaissance des ions chlorure $\mathrm{Cl}^{-}$.
– L’équation de la réaction de précipitation est : $\mathrm{Ag}^{+}+\mathrm{Cl}^{-} \longrightarrow\underbrace{(\mathrm{AgCl})}_{\downarrow} $
$>$ Conclusion :
– Le nitrate d’argent est le réactif qui permet d’identifier les ions chlorure $\mathbf{C l}^{\boldsymbol{-}}$ en solution. On obtient un précipité blanc qui noircit à la lumière.
II – Tests de reconnaissance des ions métalliques.
1 ) L’ion cuivre II ( $\mathrm{Cu}^{2+}$ ).
a) Expérience :
b ) Observation et interprétation :
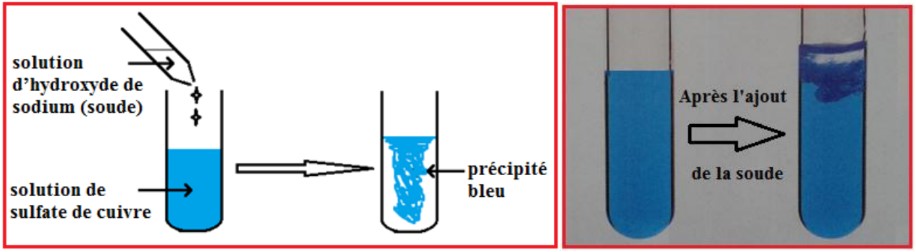
– Lorsque l’on ajoute quelques gouttes de solution d’hydroxyde de sodium (soude) $\left(\mathrm{Na}^{+}+\mathrm{HO}^{-}\right)$dans une solution contenant des ions cuivre II Cu ${ }^{2+}$ (solution de sulfate de cuivre ( $\mathrm{Cu}^{2+}+\mathrm{SO}_{4}{ }^{2-}$ ) par exemple), il se forme un précipité bleu d’hydroxyde de cuivre II Cu (OH) ${ }_{2}$.
– Cette réaction constitue le test de reconnaissance des ions cuivre II $\mathrm{Cu}^{2+}$.
– L’équation de la réaction de précipitation est : $\mathrm{Cu}^{2+}+2 \mathrm{HO}^{-} \longrightarrow \underbrace{\mathrm{Cu}(\mathrm{OH})_{2}}_{\downarrow}$
2 ) L’ion fer II ( $\mathrm{Fe}^{2+}$ ) (ion ferreux).
a) Expérience :
b ) Observation et interprétation :
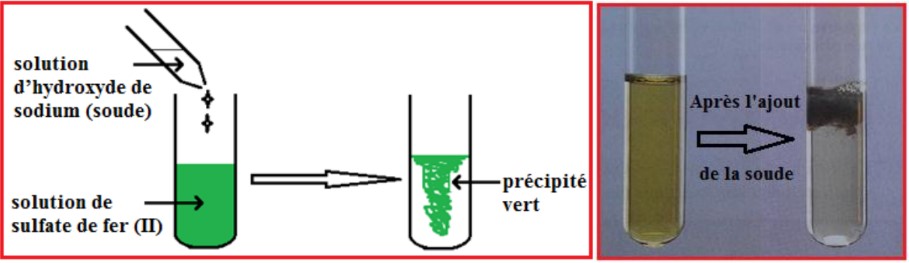
– Lorsque l’on ajoute quelques gouttes de solution d’hydroxyde de sodium (soude) $\left(\mathrm{Na}^{+}+\mathrm{HO}^{-}\right)$dans une solution contenant des ions fer II Fe ${ }^{2+}$ (solution de sulfate de fer II ( $\mathrm{Fe}^{2+}+\mathrm{SO}_{4}{ }^{2-}$ ) par exemple), il se forme un précipité vert d’hydroxyde de fer II Fe $(\mathrm{OH})_{2}$.
– Cette réaction constitue le test de reconnaissance des ions fer II Fe ${ }^{2+}$.
– L’équation de la réaction de précipitation est : $\mathrm{Fe}^{2+}+2 \mathrm{HO}^{-} \longrightarrow \underbrace{\mathrm{Fe}(\mathrm{OH})_{2}}_{\downarrow}$
3) L’ion fer III ( $\mathrm{Fe}^{3+}$ ) (ion ferrique).
a) Expérience :
b ) Observation et interprétation :
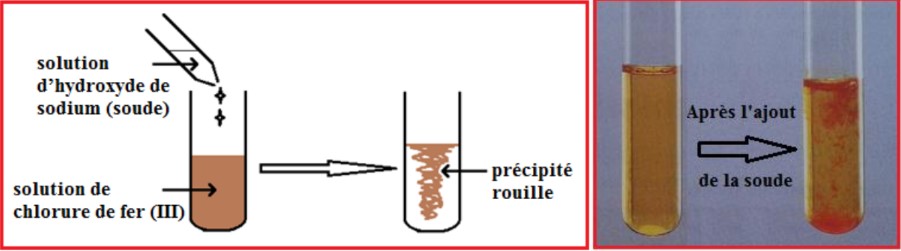
– Lorsque l’on ajoute quelques gouttes de solution d’hydroxyde de sodium (soude) $\left(\mathrm{Na}^{+}+\mathrm{HO}^{-}\right)$dans une solution contenant des ions fer III Fe ${ }^{3+}$ (solution de chlorure de fer III ( $\mathrm{Fe}^{3+}+3 \mathrm{Cl}^{-}$) par exemple), il se forme un précipité rouille d’hydroxyde de fer III Fe (OH) ${ }_{3}$.
– Cette réaction constitue le test de reconnaissance des ions fer III Fe ${ }^{3+}$.
– L’équation de la réaction de précipitation est : $\mathrm{Fe}^{3+}+3 \mathrm{HO}^{-} \longrightarrow \underbrace{\mathrm{Fe}(\mathrm{OH})_{3}}_{\downarrow}$
4) L ‘ ion Zinc $ \mathrm{Zn}^{2+}$.
a) Expérience :
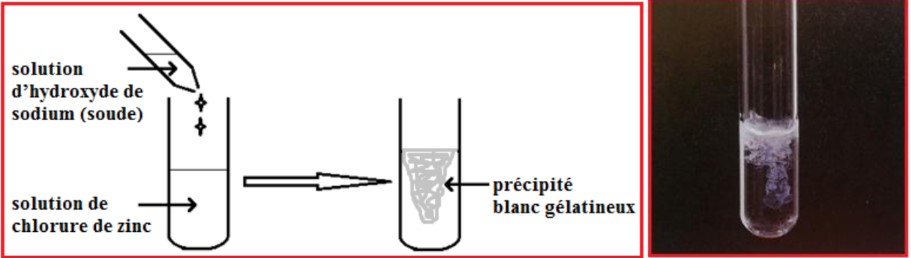
b ) Observation et interprétation :
– Lorsque l’on ajoute quelques gouttes de solution d’hydroxyde de sodium (soude) $\left(\mathrm{Na}^{+}+\mathrm{HO}^{-}\right)$dans une solution contenant des ions zinc $\mathrm{Zn}^{2+}$ (solution de chlorure de zinc ( $\mathrm{Zn}^{2+}+2 \mathrm{Cl}^{-}$) par exemple), il se forme un précipité blanc gélatineux d’hydroxyde de zinc $\mathrm{Zn}(\mathrm{OH})_{2}$.
– Cette réaction constitue le test de reconnaissance des ions zinc $\mathrm{Zn}^{2+}$.
– L’équation de la réaction de précipitation est : $\mathrm{Zn}^{2+}+2 \mathrm{HO}^{-} \longrightarrow \underbrace{\mathrm{Zn}(\mathrm{OH})_{2}}_{\downarrow}$
5 ) L’ion aluminium $\mathrm{Al}^{3+}$.
a) Expérience :
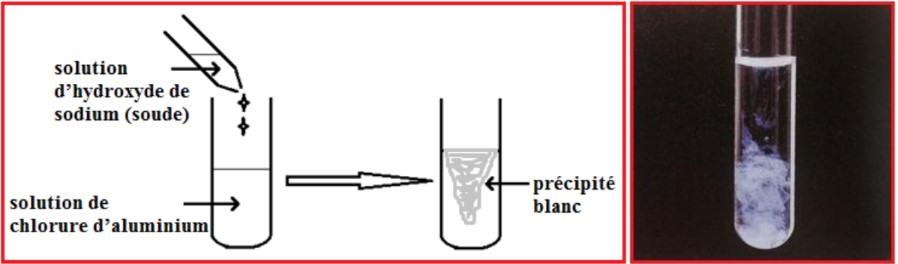
b ) Observation et interprétation :
– Lorsque l’on ajoute quelques gouttes de solution d’hydroxyde de sodium (soude) $\left(\mathrm{Na}^{+}+\mathrm{HO}^{-}\right)$dans une solution contenant des ions aluminium $\mathrm{Al}^{3+}$ (solution de chlorure $d$ ‘aluminium ( $\mathrm{Al}^{3+}+3 \mathrm{C} \ell^{-}$) par exemple), il se forme un précipité blanc d’hydroxyde d’aluminium $\mathrm{A} \ell(\mathrm{OH})_{3}$.
– Cette réaction constitue le test de reconnaissance des ions aluminium $\mathrm{Al}^{3+}$.
– L’équation de la réaction de précipitation est : $\mathrm{Al}^{3+}+3 \mathrm{HO}^{-} \longrightarrow \underbrace{\mathrm{Al}(\mathrm{OH})_{3}}_{\downarrow}$
Remarques :
– Le précipité blanc gélatineux (hydroxyde de zinc) formé avec l’ion $\mathrm{Zn}^{2+}$ est soluble dans un excès de soude et aussi dans un excès d’ammoniac.
– Le précipité blanc (hydroxyde d’aluminium) formé avec l’ion $\mathrm{Al}^{3+}$ est soluble dans un excès de soude et insoluble dans un excès d’ammoniac.
Conclusion :
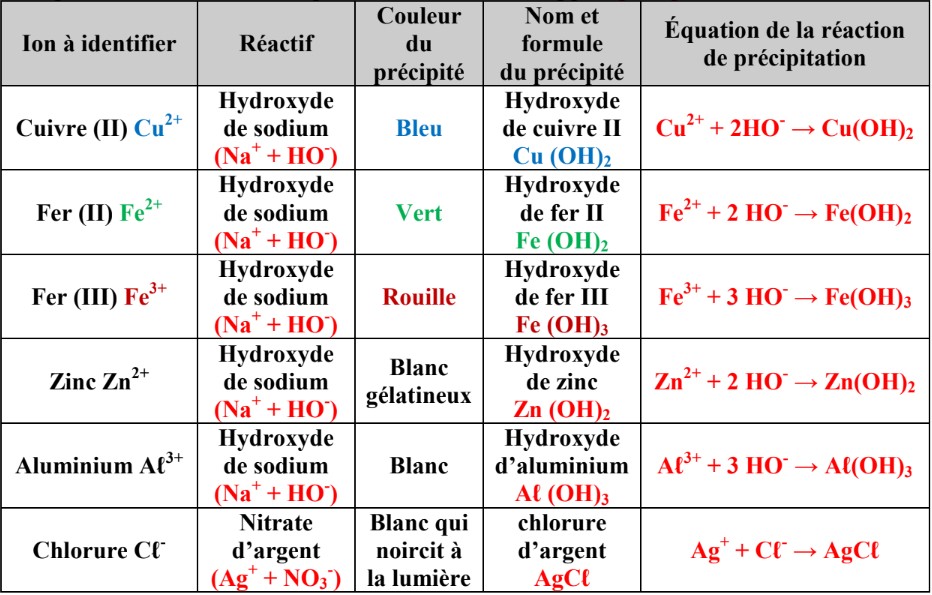
– La solution d’hydroxyde de sodium (soude) est un réactif caractéristique utilisé dans la détection des ions cuivre (II) $\mathrm{Cu}^{2+}$, fer (II) $\mathrm{Fe}^{2+}$, fer (III) $\mathrm{Fe}^{3+}$, zinc $\mathrm{Zn}^{2+}$ et aluminium $\mathrm{Al}^{3+}$.
– Un test de reconnaissance par précipitation est basée sur la transformation chimique qui a lieu entre deux ions pour former un solide appelé précipité.
III – Test de reconnaissance de l’ion sodium $\mathrm{Na}^{+}$. (facultative)
1 ) Expérience :
On trempe un fil métallique de fer ou de cuivre ou du platine dans une solution d’hydroxyde de sodium ( $\mathrm{Na}^{+}+\mathrm{HO}^{-}$) et on le place dans une flamme bleue d’un bec bunsen.

2 ) Observation :
– La flamme prend une teinte jaune quand le fil de fer a été trempé dans la solution d’hydroxyde de sodium.
3 ) Interprétation :
– La couleur jaune de la flamme est caractéristique des ions sodium $\mathrm{Na}^{+}$.
Tests de reconnaissance de quelques ions exercices corrigés
Exercice 1:
$1)$ Répond par vrai ou faux :
$a)$ précipité de couleur blanche qui noircie à la lumière confirme la présence des ions de chlorure Cl-.
$b)$ précipité de couleur vert confirme la présence des ions de fer III $\mathrm{Fe}^{3+}$.
$c)$ précipité de couleur vert confirme la présence des ions de cuivre $C u^{2+}$
$2)$ compléter les phrases:
$a)$ le gaz du $……….$ de formule chimique $……….$ brûle lorsqu’on présente une allumette enflammée à l’extrémité du tube
$b)$ l’acide chlorhydrique réagit avec les métaux : $……….$ .et $……….$ et le $……….$ mais ne réagit avec $……….$
$c)$ hydroxyde de sodium réagit avec les métaux: $……….$ et $……….$ et ne réagit pas avec les métaux $……….$ et $……….$
$1)$
$a)$ Vrai
$b)$ Faux
$c)$ Faux
$2)$
$a)$ le gaz du dihydrogène de formule chimique $\mathrm{H}_{2}$ brûle lorsqu’on présente une allumette enflammée à l’extrémité du tube
$b)$ l’acide chlorhydrique réagit avec les métaux : Zinc .et Fer et L’aluminium mais ne réagit avec Cuivre
$c)$ hydroxyde de sodium réagit avec les métaux: Aluminium et Zinc et ne réagit pas avec les métaux Cuivre et Fer
Exercice 2:
$1)$ Associez chaque solution à sa formule chimique correspondante :
¤ Les solutions :
• Hydroxyde de sodium
• Nitrate d’argent
• Chlorure de zinc
• Chlorure de fer III
• Chlorure d’aluminium
• Sulfate de cuivre
• Sulfate de fer II
¤ Les formules chimiques :
• $\left(\mathrm{Na}^{+}+\mathrm{HO}^{-}\right)$
• $\left(\mathrm{Ag}^{+}+\mathrm{NO}_{3}^{-}\right).$
• $\left(\mathrm{Cu}^{2+}+\mathrm{SO}_{4}^{2-}\right)$
• $\left(\mathrm{Fe}^{2+}+\mathrm{SO}_{4}^{2-}\right)$
• $\left(\mathrm{Fe}^{3+}+3 \mathrm{Cl}^{-}\right)$
• $\left(\mathrm{Zn}^{2+}+2C l^{-}\right.$
• $\left(\mathrm{Al}^{3+}+3 \mathrm{Cl}^{-}\right)$
Exercice 3:
Compléter le tableau :
| Ion | Formule chimique |
|---|---|
| sodium | ……………….. |
| chlorure | ……………….. |
| ……………….. | Cu²⁺ |
| Fer II | ……………….. |
| ……………….. | Fe³⁺ |
Exercice4:
Karim à réaliser les expériences suivantes :
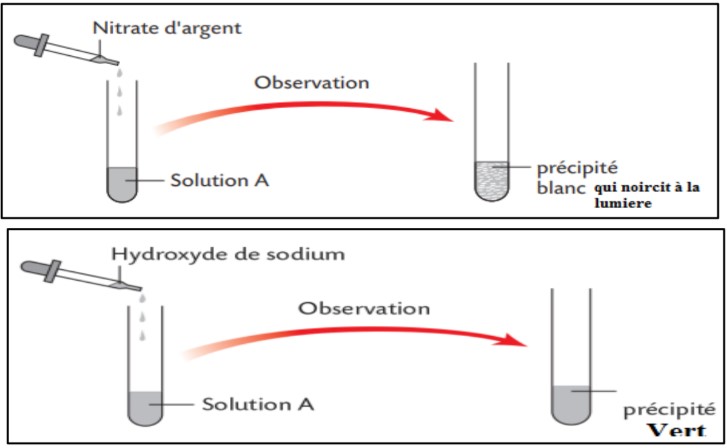
$1)$ Donner formule chimique de solution de nitrate d’argent
$2)$ Donner formule chimique de solution d’hydroxyde de sodium
$3)$ Quelles conclusions peut tu-tirer des observations de Karim dans l’expérience $1$
$4)$ Quelles conclusions peut tu-tirer des observations de Karim dans l’expérience $2$
Exercice 5:
Khalid à réaliser les expériences suivantes :
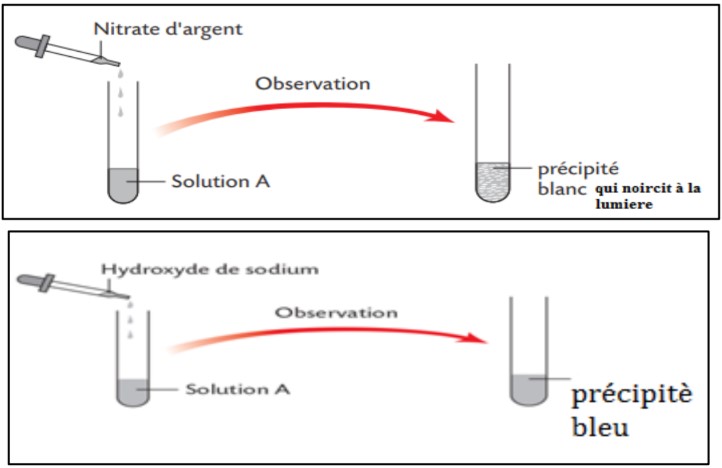
$1)$ Quelles conclusions peut tu-tirer des observations de Khalid dans l’expérience $1$
$2)$ Quelles conclusions peut tu-tirer des observations de Khalid dans l’expérience $2$
Exercice 6:
On introduit $2$ plaques métalliques $\mathbf{A}$ et $\mathbf{B}$ dans 2 béchers contenant une solution d’acide chlorhydrique.
On observe l’émission d’un gaz dans le bécher qui contient la plaque $A$, par contre rien ne se produit dans l’autre bécher.
$1)$ Donner le nom du gaz produit.
$2)$ On ajoute des gouttes de la solution de soude dans le bécher qui contient la plaque $A$ et on observe la formation d’un précipité gélatineux blanc.
$a)$ Donner le nom de ce précipité.
$b)$ En déduire le métal formant la plaque $A$ .
$3)$ La plaque $B$ est caractérisée par une couleur rouge brique, quel est le métal qui constitue cette plaque?
Exercice 7:
Une plaque d’aluminium réagit avec une quantité d’acide chlorhydrique en produisant un gaz incolore qui détonne à l’approche d’une flamme.
$1)$ Quel est le nom et la formule chimique du gaz produit?
$2)$ On ajoute à la solution obtenue des gouttes de soude et on observe la formation d’un précipité blanc.
$a)$ Donner le nom du précipité blanc.
$b)$ En déduire le nom et la formule chimique de l’ion détecté.
$3)$ Écrire le bilan de la réaction d’aluminium avec la solution d’acide chlorhydrique.
$4)$ Écrire l’équation équilibrée de la précipitation.
Exercice 8:
Soit une solution $(S)$ contenant $2$ ions. Afin d’identifier ces 2 ions:
$A.$ On ajoute, à une quantité de cette solution, un peu de la soude ( $\mathrm{Na}^{+}+\mathrm{OH}^{-}$) et on observe la formation d’un précipité de couleur rouille.
$1)$ Donner le nom et la formule moléculaire du précipité.
$2)$ Écrire l’équation de la réaction chimique de précipitation.
$3)$ En déduire le nom de l’ion détecté et donner son symbole.
$B.$ On ajoute à l’autre quantité de la solution $( S )$ des gouttes de nitrate d’argent ( $\mathrm{Ag}^{+}+\mathrm{NO}_{3}^{-}$) et on observe la formation d’un précipité blanc qui noircit à la lumière.
$1)$ Donner le nom et la formule moléculaire du précipité blanc.
$2)$ Écrire l’équation de la réaction chimique de précipitation.
$3)$ En déduire le nom de l’ion détecté et donner son symbole.
$C.$ A partir des deux expériences $A$ et $B$ donner le nom et la formule ionique de la solution $(\mathrm{S})$.
Exercice 9:
On verse une quantité de la soude dans une solution $(S)$ et on observe la formation d’un précipité blanc gélatineux.
$1)$ Donner le nom du précipité et sa formule chimique.
$2)$ Donner le nom de l’ion détecté et son symbole.
$3)$ Quel est l’ion détecteur ?
$4)$ Écrire l’équation chimique de la précipitation.
Exercice 10:
Afin de préparer une solution $(S)$, on verse une quantité de poudre d’un métal $X$ dans un tube à essai qui contient une solution (Y). on constate qu’un gaz se dégage.
$1)$ Quel est le gaz dégagé et sa formule chimique ?
$2)$ Comment on peut détecter ce gaz ?
On réalise $2$ manipulations :
* Manipulation $1$ :
On verse une quantité de la solution du nitrate d’argent dans la solution $(Y)$, on observe la formation d’un précipité blanc qui noircit à la lumière.
$1)$ Donner le nom du précipité qui se forme et sa formule chimique.
$2)$ Donner la formule ionique de la solution du nitrate d’argent.
$3)$ Quel est l’ion détecté, donner sa formule chimique.
$4)$ Écrire l’équation chimique de la précipitation.
$5)$ En déduire le nom de la solution $(Y)$ et donner sa formule chimique.
* Manipulation $2$ :
On verse une quantité de la solution de soude dans la solution $(S)$, on observe la formation d’un précipité blanc.
$1)$ Donner le nom du précipité qui se forme et sa formule chimique.
$2)$ Déterminer l’ion détecteur.
$3)$ Écrire l’équation chimique de la précipitation.
$4)$ En déduire le nom de la solution $(X)$ et donner sa formule chimique.
$5)$ En déduire la nature du métal $X$.
$6)$ Écrire l’équation simplifier de la réaction d’acide chlorhydrique avec le métal $X$.
Tests de reconnaissance de quelques ions exercices corrigés
