Extraction-séparation et identification des espèces chimiques
Exercice 1: (questions de cours)
Cocher la (ou les) réponse(s) exacte(s):
- Lorsque deux liquides ne sont pas miscibles, celui qui a la plus grande densité :
- Lors d’une extraction liquide – liquide, l’espèce chimique à extraire doit:
- Une hydrodistillation:
- Pour extraire une espèce chimique dissoute dans de l’eau, le solvant d’extraction doit être:
- Lors d’une chromatographie, l’éluant permet de:
- Lors de la réalisation d’une chromatographie, la ligne de dépôt doit être:
- Le rapport frontal s’exprime en:
- À sa température de fusion, une espèce chimique passe de:
1. Liquides non miscibles et densité
Réponse correcte :
Le liquide le plus dense se place en dessous du liquide moins dense lorsqu’ils ne sont pas miscibles.
2. Extraction liquide-liquide
Réponse correcte :
Pour une extraction efficace, l’espèce doit avoir une affinité plus grande pour le solvant extracteur.
3. Hydrodistillation
Réponse correcte :
L’hydrodistillation utilise la vapeur d’eau pour entraîner des composés non miscibles avec l’eau.
4. Solvant d’extraction
Réponses correctes :
Le solvant doit former deux phases distinctes avec l’eau pour permettre la séparation.
5. Rôle de l’éluant en chromatographie
Réponse correcte :
L’éluant entraîne les espèces à différentes vitesses selon leurs affinités avec la phase stationnaire.
6. Ligne de dépôt en chromatographie
Réponse correcte :
Le dépôt ne doit pas être immergé dans l’éluant pour éviter la dissolution directe des espèces.
7. Unité du rapport frontal
Réponse correcte :
Le rapport frontal est le quotient de deux distances, c’est donc une grandeur sans unité.
8. Température de fusion
Réponse correcte :
La fusion correspond au passage de l’état solide à l’état liquide sous l’effet de la chaleur.
Résumé des techniques
| Technique | Principe | Application |
|---|---|---|
| Extraction liquide-liquide | Différence de solubilité | Séparation de composés |
| Hydrodistillation | Entraînement à la vapeur | Extraction d’huiles essentielles |
| Chromatographie | Différence d’affinité | Analyse de mélanges |
Exercice 2: Le choix d’un solvant
On désire extraire le diode de l’eau iodée. La solubilité du diode dans différents solvants est donnée dans le tableau suivant :
| Solvant | Eau | Alcool | Ether | Benzène |
|---|---|---|---|---|
| Solubilité du diode (g/L) | 0,3 | 250 | 250 | 140 |
| Densité | 1,0 | 0,8 | 0,71 | 0,88 |
| Température d’ébullition (°C) | 100 | 78 | 35 | 80 |
Informations complémentaires :
- L’alcool est miscible à l’eau
- L’éther et le benzène ne sont pas miscibles à l’eau
- Rechercher la définition du mot « solubilité ».
- Quel solvant vaut-il mieux choisir pour extraire le diode de l’eau iodée? Justifier ta réponse.
- Dresser le protocole de cette extraction (verrerie à utiliser, mode opératoire)
- Quelle phase faut-il recueillir? Où se trouve-t-elle ?
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 3: Extraction de la vanilline
L’arôme de vanille vendu dans le commerce est composé essentiellement de trois espèces chimiques : la vanilline, l’acide vanillique et l’acide p-hydroxybenzoïque.
- L’arôme de vanille est-il une espèce chimique pure ou un mélange ?
- À l’aide des indications ci-dessous (Donnée), faire un schéma de l’ampoule à décanter et préciser la position et le contenu de chaque phase. Justifier.
- De quel type d’extraction s’agit-il ? Quel est le rôle du chloroforme ?
- Quelles sont les opérations à effectuer après la séparation des phases contenues dans l’ampoule pour isoler la vanilline pure ?
Données :
- La vanilline est très soluble dans le chloroforme et peu soluble dans l’eau.
- L’acide vanillique et l’acide p-hydroxybenzoïque sont solubles dans l’eau.
- La densité du chloroforme est de 1,47.
- Température d’ébullition : chloroforme (61°C), vanilline (154°C).
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 4: Extraction de l’huile essentielle de lavande
L’extraction de l’huile essentielle de lavande s’effectue à l’aide d’un montage à l’entraînement à la vapeur (ou hydrodistillation).
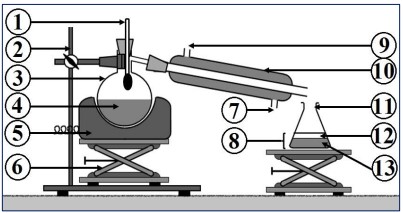
- Nommer les différentes parties du montage en utilisant les termes suivants :
Chauffe-ballon; Ballon à fond rond; Support; Distillat; Réfrigérant à eau; Arrivée d’eau froide; Sortie d’eau tiède; thermomètre; lavande avec l’eau; Support élévateur; Erlenmeyer; Phase supérieure; Phase inférieure.
- Quel est le rôle de la vapeur d’eau ? Celui du réfrigérant à eau ?
- Représenter le contenu de l’erlenmeyer après l’hydrodistillation. Justifier.
- Quel est l’intérêt d’ajouter de l’eau salée ?
- A l’aide des données du tableau, quel solvant extracteur peut-on choisir ? Justifier.
- Représenter l’ampoule à décanter après décantation. Légender en justifiant.
Données :
| Solubilité dans : | Eau | Eau salée | Cyclohexane | Ether éthylique |
|---|---|---|---|---|
| Huile essentielle | Faible | Très faible | Très élevée | Élevée |
| Densité (d) | 1,00 | 1,13 | 0,78 | 0,71 |
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 5: Informations concernant un solvant
L’étiquette d’un flacon d’éthanol présente les informations ci-après :
ETHANOL
Alcool éthylique C2H5OH
\[ M = 46,07 \, \text{g/mol} \]
\[ d = 0,79 \]
\[ T_{éb} = 78,5^\circ \text{C} \]
On souhaite vérifier la densité de l’éthanol. On dispose pour cela d’une balance, d’éprouvettes graduées, de béchers et d’un flacon d’éthanol.
- Préciser les mesures de sécurité à respecter pour manipuler sans danger l’éthanol.
- Proposer un protocole permettant de déterminer la densité de l’éthanol.
- Lors d’une expérience, on a trouvé qu’un volume V = 20 mL d’éthanol a une masse m = 15,8 g, alors que le même volume d’eau a une masse m = 20,0 g. En déduire la densité de l’éthanol par rapport à l’eau.
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 6: Chromatographie de l’huile essentielle de lavande
On analyse par chromatographie sur couche mince l’huile essentielle de lavande. On a obtenu le chromatogramme ci-dessous avec les produits suivants :
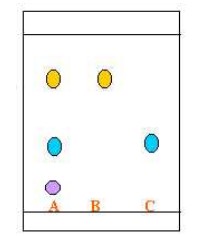
Produits analysés :
- A : huile essentielle de lavande
- B : linalol
- C : acétate de linalyle
A partir du chromatogramme, dire, en justifiant la réponse :
a) Quels sont le(s) produit(s) pur(s)
b) Quels sont le(s) produit(s) composé(s)
- Quels sont les buts d’une chromatographie ?
- Quelles molécules peuvent être identifiées dans l’huile essentielle de lavande ? Justifier.
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 7: Analyse par chromatographie
1. On réalise une chromatographie de trois encres : une encre verte (B), une encre violette (C) et une encre noire (A). Le chromatogramme obtenu est donné ci-dessous.
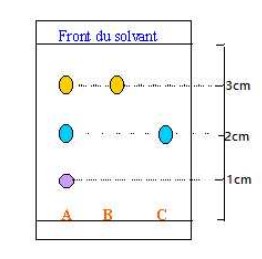
En analysant le chromatogramme, que pouvez-vous dire sur les encres testées ? Utiliser les expressions ou mots :
- Corps pur
- Corps composé
- Corps pur(s) commun(s)
- Rapport frontal
2. Déterminer le rapport frontal de la tache correspondant à l’encre C.
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 8: Analyse par chromatographie
On a réalisé la chromatographie de deux échantillons A et B, et d’un cops pur servant de référence noté R (menthone).
L’étude du chromatogramme a permis de repérer lespositions des différentes tache après révélation.
• Front du solvant :8,0 cm
• Echantillon A : on relève deux taches situées à 3,0 cm et 5,0 cm de la ligne de base.
• Référence (menthone) : \[ R_f = 0,\!75 \]
1-dessiner le chromatogramme.
2-Cette chromatographie permet-elle d’identifier un ou plusieurs corps pur contenus dans les échantillons A et B.
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 9: Chromatographie sur une couche mince d’une huile essentielle
On effectue la chromatographie sur une couche mince (CCM) de l’huile essentielle depeaux d’oranges.
On réalise les dépôts suivants :
*dépôt 1 : Limonine
*dépôt 2 : Linalol
*dépôt 3 : Citral
*dépôt 4 : huile essentielle de peaux d’orange
La plaque est placée, verticalement, dans un fond d’éluant. Après élution et révélation, on obtient le chromatogramme ci-dessus.
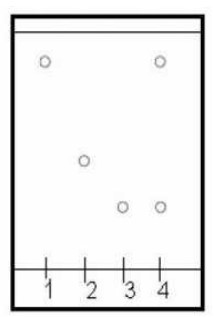
1- Quel est le rôle de l’éluant ?
2- Les espèces déposées sont incolores. Que doit faire l’expérimentateur pour révéler le chromatogramme ?
3- Quels sont les constituants de l’huile essentielle de peaux d’orange ?
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 10: Choix du solvant pour extraire diiode
L’huile essentielle de girofle est extraite des boutons floraux séchés du giroflier, communément appelés clous de girofle. Quant à l’huile essentielle de giroflier, elle est produite à partir des feuilles et des rameaux de la même plante. Selon une brochure sur les essences naturelles végétales, ces deux huiles, utilisées en parfumerie et en pharmacie, présentent des compositions distinctes : toutes deux contiennent de l’eugénol, mais l’huile de girofle se différencie par la présence supplémentaire d’un ester de l’eugénol, l’acétate (ou éthanoate) d’eugényle. Cet ester n’étant pas disponible dans le commerce, un élève décide d’en réaliser la synthèse afin de confirmer les informations de la brochure concernant la composition des huiles de girofle et de giroflier.
Après avoir fabriqué l’ester d’eugénol il place sur une plaque de silice, sensible aux
UV, les dépôts de quatre solutions : – Une d’eugénol : E
– Une d’ester d’eugénol préparé par l’élève : O
– Une d’essence de girofle obtenue des clous de girofles : C
– Une d’essence de girofle obtenue à partir des feuilles et rameaux du giroflier : F Après élution, l’élève obtient le chromatogramme ci-dessous :

1- Calculer le rapport frontal de l’ester de l’eugénol.
2- L’élève peut-il confirmer ce qui est marqué sur la brochure ?
3- Peut-t-on aussi différencier l’essence de girofle et l’essence de giroflier ?
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 11: Etude de l’heptane
L’heptane est un solvant non miscible à l’eau. Le volume = 25,0 mL d’heptane pèse une masse m = 18,5 g.
1. Calculer la masse volumique ρ de l’heptane en g.mL-1 et en kg.m-3.
2. Quelle est sa densité d par rapport à l’eau ?
3. Dans un tube à essai on trouve un mélange d’heptane et d’eau. Représenter le tube à essai en indiquant où se trouve chaque liquide.
4. Calculer la masse m1 en gramme correspondant à un volume V1 = 50,0 mL d’heptane.
5. Calculer le volume V2 en dL correspondant à une masse m2 = 1,50 kg d’heptane.
Donnée : ρeau = 1 g.cm-3
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Exercice 12: Densité de l’acétone et du mercure
On mesure à l’éprouvette un volume de V = 100 mL d’acétone. Cette quantité d’acétone pèse m = 79,2 g.
1. Calculer la masse volumique ρA de l’acétone en g/cm3 puis en kg/m3.
2. En déduire la densité dA de l’acétone.
Le mercure (Hg) est le seul métal à l’état liquide à la température ambiante. Sa densité vaut d = 13,5.
3. Quelle est la masse d’un litre de mercure ? On calculera dans un premier temps la masse volumique du mercure ρHg.
4. Quel est le volume V1 occupé par m1 = 1 kg de mercure ?
Données : ρeau = 1 kg/dm3 = 1 kg.dm-3
🔒 Abonnez-vous pour accéder à la correction détaillée en texte .
Extraction-séparation et identification des espèces chimiques
