La géométrie de quelques molécules – Cours
Géométrie de quelques molécules
I – Règles de duet et de l’octet
1. Structure des gaz rares
| Atome | Numéro atomique | Structure électronique | Couche externe |
|---|---|---|---|
| \( He \) Hélium | \( Z = 2 \) | \((K)^2\) | \((K)^2\) |
| \( Ne \) Néon | \( Z = 10 \) | \((K)^2(L)^8\) | \((L)^8\) |
| \( Ar \) Argon | \( Z = 18 \) | \((K)^2(L)^8(M)^8\) | \((M)^8\) |
Les gaz rares (ou gaz inertes) ne participent pas à des transformations chimiques, ils sont chimiquement stables, leurs couches externes sont saturées.
2. La règle du duet
Au cours des transformations chimiques, les éléments chimiques de numéro atomiques (\( Z \leq 4 \)) évoluent de manière à acquérir la structure électronique de l’hélium, ils ont deux électrons sur la couche externe.
3. La règle de l’octet
Au cours des transformations chimiques, les éléments chimiques de numéro atomiques (\( 5 \leq Z \leq 18 \)) évoluent de manière à acquérir la structure électronique de Néon ou de l’Argon. Ils portent 8 électrons sur leur couche externe.
Exemple :
| L’atome | Structure électronique de l’atome | Structure électronique stable | Formule de l’ion |
|---|---|---|---|
| \( Li : Z = 3 \) | \((K)^2(L)^1\) | \((K)^2\) | \( Li^+ \) |
| \( Mg : Z = 12 \) | \((K)^2(L)^8(M)^2\) | \((K)^2(L)^8\) | \( Mg^{2+} \) |
| \( F : Z = 9 \) | \((K)^2(L)^7\) | \((K)^2(L)^8\) | \( F^- \) |
| \( O : Z = 8 \) | \((K)^2(L)^6\) | \((K)^2(L)^8\) | \( O^{2-} \) |
II – La représentation de Lewis d’une molécule
1. La molécule
La molécule est des assemblages des atomes attachés les uns des autres.
La molécule est stable et électriquement neutre.
2. Liaison de covalente simple
Une liaison covalente simple est la mise en commun de deux électrons entre deux atomes, le doublet commun est appelé doublet liant (chaque atome y participe par un électron).
Remarque :
On représente La liaison covalente par un trait (–) entre les symboles de deux atomes.
Exemples :
Liaison covalente simple : H – H
Liaison covalente double : O = O
Liaison covalente triple : N ≡ N
3. La représentation de Lewis d’une molécule
La représentation de Lewis d’une molécule est une représentation des atomes et de tous les doublets d’électrons (liants et non–liants) de cette molécule.
Méthode de détermination de la représentation de Lewis d’une molécule :
- Ecrire la structure électronique de chaque atome.
- Déterminer le nombre global nt d’électrons de couches externes de chaque atome dans la molécule.
- Déterminer le nombre global nd de doublet d’électrons : \( n_d = \frac{ n_t}{2} \).
- Déterminer le nombre \( n_L \) de liaison covalente que doit établir chaque atome pour acquérir une structure en octet (8–p) ou en duet (2–p) avec p est le nombre d’électrons d’équivalence.
- Déterminer le nombre nd de doublet non liants de chaque atome :
\[ n_d’ = \frac{p – n_L}{2} \]
Exemple : représenter le modèle de Lewis des molécules suivantes
| Molécule | structure électronique | Nombre global d’é | Nombre global de doublet d’é | Nombre de liaison covalente | Nombre de doublet non liants | Représentation de Lewis |
|---|---|---|---|---|---|---|
| \( HC\ell \) | \( H: (K)^1 \) \( C\ell: (K)^2(L)^8(M)^7 \) | \( n_t = 1 + 7 \) \( n_t = 8 \) | \( n_d = \frac{n_t}{2} \) \( n_d = 8 \) | \( H: 2 – 1 = 1 \) \( C\ell: 8 – 7 = 1 \) | \( H: \frac{1 – 1}{2} = 0 \) \( C\ell: \frac{7 – 1}{2} = 3 \) | H-Cl avec 3 doublets non liants sur Cl
|
| \( CH_4 \) | \( H: (K)^1 \) \( C: (K)^2(L)^4 \) | \( n_t = 4 + 4 \) \( n_t = 8 \) | \( n_d = \frac{8}{2} \) \( n_d = 4 \) | \( H: 2 – 1 = 1 \) \( C: 8 – 4 = 4 \) | \( H: \frac{1 – 1}{2} = 0 \) \( C: \frac{4 – 4}{2} = 0 \) | C avec 4 liaisons simples vers H
|
| \( NH_3 \) | \( H: (K)^1 \) \( N: (K)^2(L)^5 \) | \( n_t = 3 + 5 \) \( n_t = 8 \) | \( n_d = \frac{8}{2} \) \( n_d = 4 \) | \( H: 2 – 1 = 1 \) \( N: 8 – 5 = 3 \) | \( H: \frac{1 – 1}{2} = 0 \) \( N: \frac{5 – 3}{2} = 1 \) | N avec 3 liaisons simples vers H et 1 doublet non liant
|
| \( CO_2 \) | \( C: (K)^2(L)^4 \) \( O: (K)^2(L)^6 \) | \( n_t = 4 + 2 \times 6 \) \( n_t = 16 \) | \( n_d = \frac{16}{2} \) \( n_d = 8 \) | \( C: 8 – 4 = 4 \) \( O: 8 – 6 = 2 \) | \( C: \frac{4 – 4}{2} = 0 \) \( O: \frac{6 – 2}{2} = 2 \) | O = C = O avec 2 doublets non liants sur chaque O
|
III – Isomères
1. Les formules des molécules
Formule brute : indique le symbole et le nombre des atomes présents.
Exemple : \( C_2H_6O \)
Formule développée : elle fait apparaître toutes les atomes et toutes les liaisons entre les atomes de la molécule.
Exemple :
H
|
H-C-C-O-H
|
H
Formule semi-développée : indique les types de liaison entre les atomes principaux.
Exemple :
\[CH_3 – CH_2 – OH\]
2. Isomère
Des isomères sont des composés qui ont mêmes formules brutes mais des formules développées différentes (qui ont des propriétés physiques et chimiques différentes).
Exemple :
La formule brute \( C_2H_6O \) donne deux isomères :
L’éthanol : \( CH_3 – CH_2 – OH \) et l’oxyde de diméthyle : \( CH_3 – O – CH_3 \)
IV – Géométrie des molécules
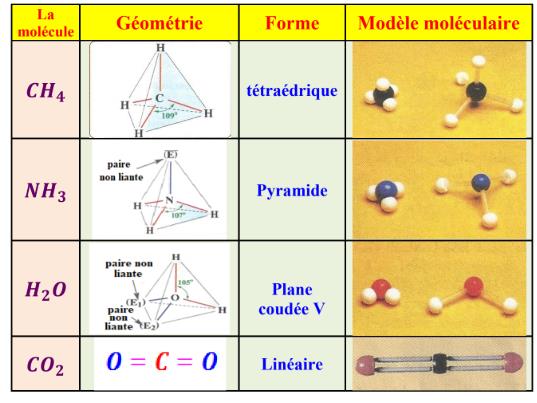
1. Géométrie spatiale des molécules
La géométrie de la molécule résulte des répulsions entre les doublets liants et non liants qui se repoussent au maximum les uns des autres et la molécule prend une certaine disposition spatiale.
On trouve un atome central relié avec d’autres atomes par des liaisons covalentes.
2. Représentation de Cram
La représentation de Cram donne un aperçu de la configuration spatiale des atomes qui composent une molécule. Elle fait apparaître les liaisons en perspective :
| Liaison située dans le plan de la feuille : | |
| Liaison située en avant du plan de la feuille : | |
| Liaison située en arrière du plan de la feuille : |
Exemple :
Molécule de méthane :
| Molécule de méthane \( CH_4 \) | 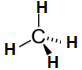 |
|---|---|
| Molécule d’éthane \( CH_3 – CH_3 \) | 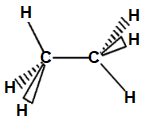 |
La géométrie de quelques molécules – Cours