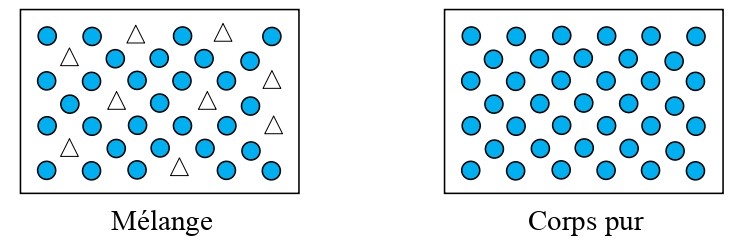
Introduction
L’étude de le corps pur et ses caractéristiques en (1AC) permet aux élèves de comprendre la diversité des matériaux qui nous entourent et de reconnaître les caractéristiques spécifiques de chaque substance.
Cela inclut des propriétés telles que la masse, le volume, la densité, le point de fusion, le point d’ébullition et la solubilité .
I – Température d’un mélange lors de l’ébullition et la fusion :
1 – Lors de l’ébullition :
Expérience :
On chauffe une quantité d’eau salée, on relève la température du mélange à des dates différentes tout en suivant l’état physique de l’eau.
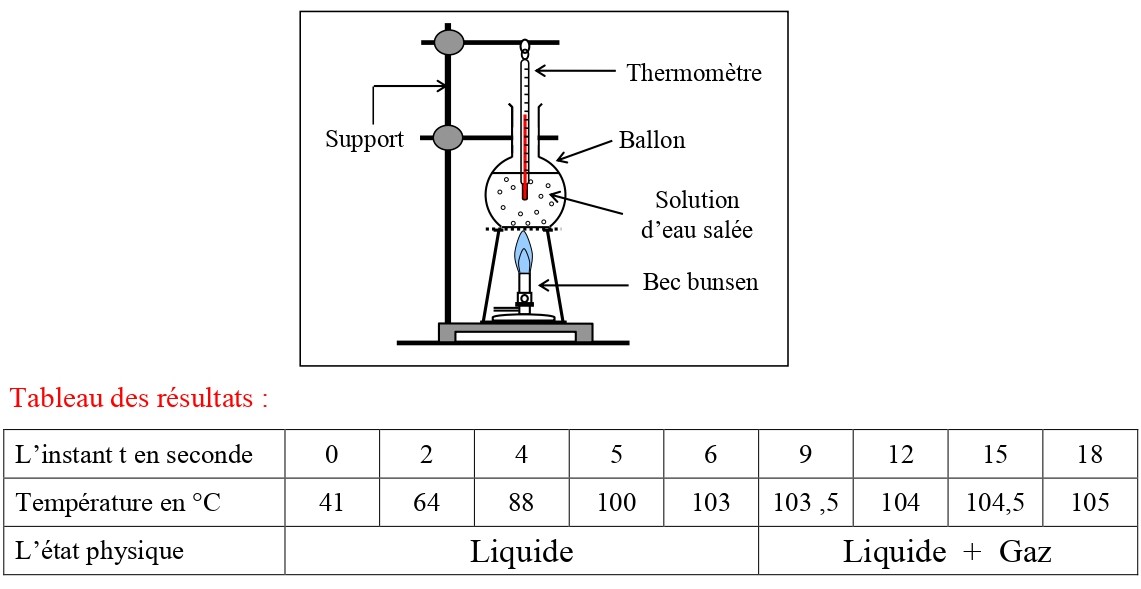
A laide des résultats obtenus dans le tableau ci-dessus, on trace la courbe représentant la variation de la température en fonction du temps.
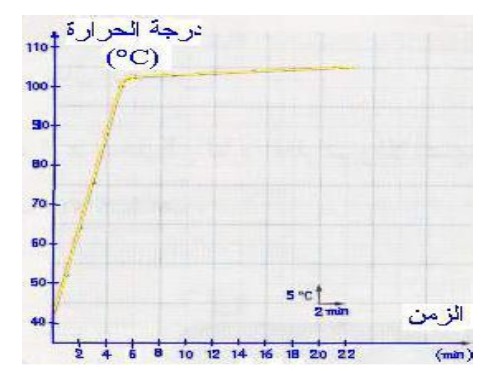
A partir de la courbe ci-contre, on constate que la température du mélange augmente rapidement durant le chauffage jusqu’à l’arriver à la température 103°C, tandis qu’au moment du changement d’état physique ( la vaporisation ), la température augmente toujours mais de façon lente.
2 – Lors de la fusion :
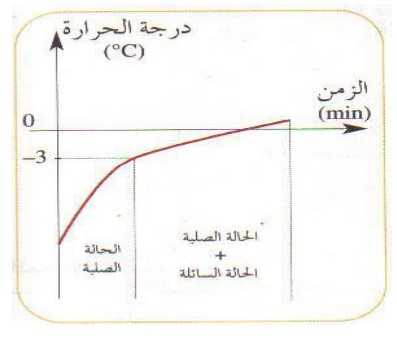
La courbe ci-dessous représente la variation de la température d’eau salée lors de sa fusion.
A partir de la courbe ci-contre, on constate que la température du mélange augmente rapidement durant le chauffage jusqu’à l’arriver à la température – 3°C, tandis qu’au moment du changement d’état physique ( la fusion ), la température augmente toujours mais de façon lente.
Résumé :
La température d’un mélange varie lentement durant le changement d’état physique.
II – Température de l’eau lors de l’ébullition et la fusion :
1 – Lors de l’ébullition :
Expérience :
On chauffe une quantité d’eau pure dans un ballon ouvert, on relève la température à des dates différentes tout en suivant l’état physique de l’eau.
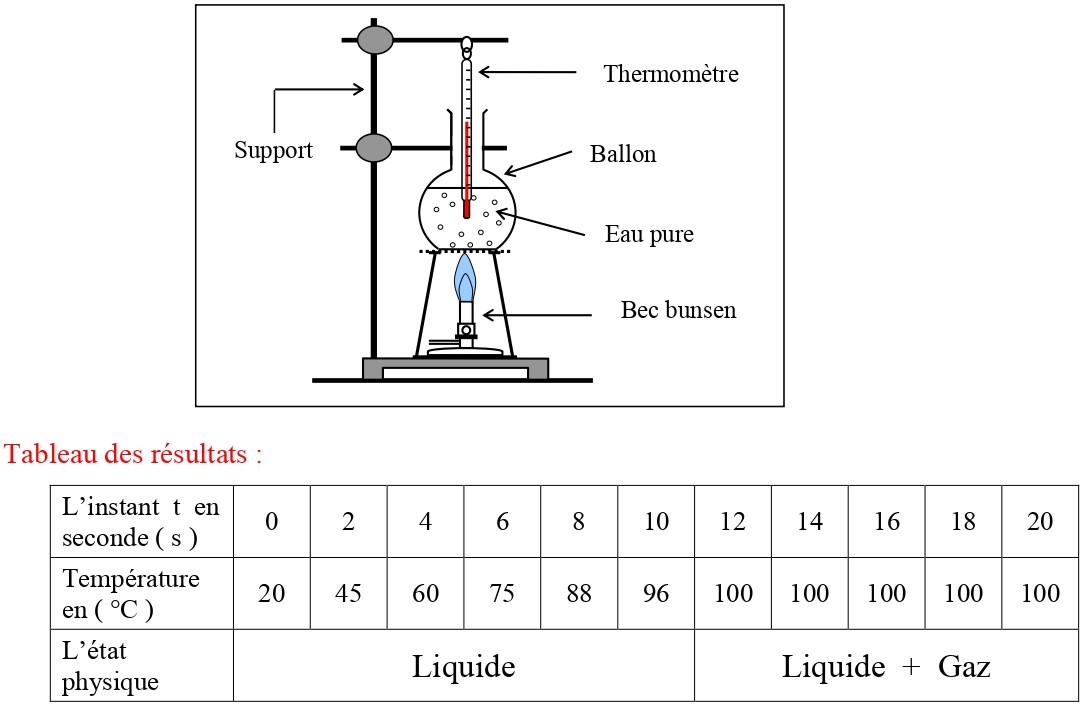
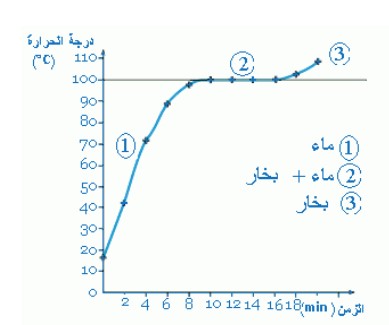
A laide des résultats obtenus dans le tableau ci-dessus, on trace la courbe représentant la variation de la température en fonction du temps.
A partir de la courbe ci-contre, on constate que la température de l’eau pure augmente rapidement durant le chauffage sans avoir un changement d’état physique, lorsque la température atteint 100°C, cette valeur reste constante durant le changement d’état physique ( la vaporisation ).
2 – Lors de la fusion :
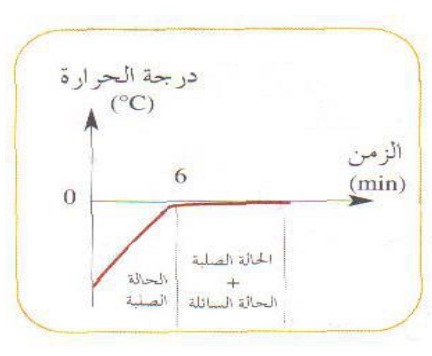
La courbe ci-contre représente la variation de la température durant le chauffage d’un moreau de glace constitué d’eau pure. On constate que la température de l’eau pure augmente sans changement d’état physique.
Lorsque la température atteint 0°C, cette valeur reste constante durant le changement d’état physique ( la fusion ).
Résumé :
Sous la pression atmosphérique normale, lors de l’ébullition de l’eau pure, la température reste constante sur 100°C qu’on l’appelle température d’ébullition de l’eau pure.
– Sous la pression atmosphérique normale, lors de la fusion de la glace pure, la température reste constante sur 0°C qu’on l’appelle température de fusion de l’eau pure.
– Sous la pression atmosphérique normale, la température de fusion 0°C et la température d’ébullition 100°C sont deux caractéristique de l’eau pure.
III – Les caractéristiques d’un corps pur :
Les températures de fusion ( ou de solidification ) et d’ébullition ( ou condensation liquide ) sont parmi les caractéristiques d’un corps pur.
Exemple :
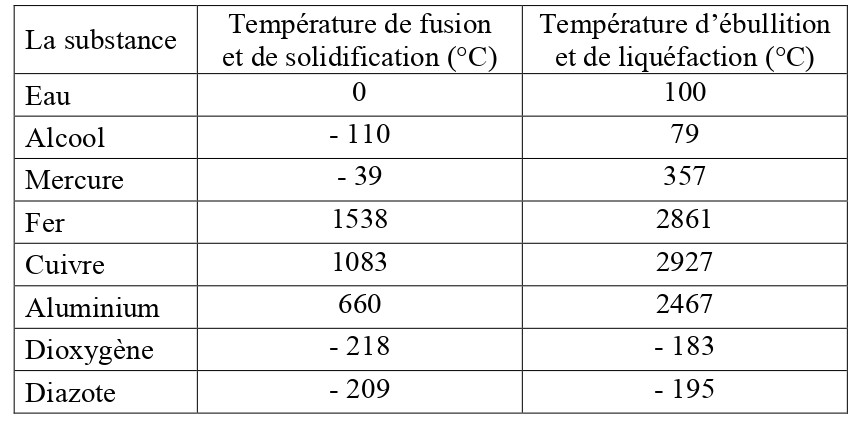
Voir aussi